Não consegui resolver o problema abaixo, se alguém puder resolver fico muito grato, obrigado.
(Exercício formulado pelo professor): 14) Um composto orgânico, quando analisado, apresentou a seguinte composição elementar emtermos de massa: 55,8% de C, 7,0% de H e 37,2% de O. Uma amostra de 1,5 g deste composto, quando vaporizada, ocupa 550 cm3 e exerce uma pressão de 740 Torr a 100°C. Determine a fórmula molecular do composto.
A resposta que obtive trabalhando apenas em cima das fórmulas percentual e mínima foi absurda, inconsistente.
Química Geral ⇒ Fórmula Molecular, mínima e percentual + Teoria dos gases
Jun 2015
28
20:20
Fórmula Molecular, mínima e percentual + Teoria dos gases
Editado pela última vez por mfjunior em 28 Jun 2015, 20:20, em um total de 1 vez.
- VALDECIRTOZZI

- Mensagens: 2569
- Registrado em: 04 Ago 2008, 17:08
- Última visita: 13-10-20
- Agradeceu: 197 vezes
- Agradeceram: 1590 vezes
Set 2015
11
08:51
Re: Fórmula Molecular, mínima e percentual + Teoria dos gase
Pela equação de Clayperon:
1 torr = 1mmHg
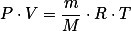


Em 100 g do composto temos:

Dividindo pela massa molar de cada átomo:


Dividindo tudo pelo menor valor (2,325):

A fórrmula mínima é , cuja massa molar é 43 g/mol, Como a massa molar do composto é o dobro da massa molar da fórmula mínima, a fórmula molecular do composto é:
, cuja massa molar é 43 g/mol, Como a massa molar do composto é o dobro da massa molar da fórmula mínima, a fórmula molecular do composto é:

Espero ter ajudado!
1 torr = 1mmHg
Em 100 g do composto temos:
Dividindo pela massa molar de cada átomo:
Dividindo tudo pelo menor valor (2,325):
A fórrmula mínima é
Espero ter ajudado!
Editado pela última vez por VALDECIRTOZZI em 11 Set 2015, 08:51, em um total de 1 vez.
So many problems, so little time!
-
- Tópicos Semelhantes
- Resp.
- Exibições
- Últ. msg
-
- 2 Resp.
- 1323 Exibições
-
Últ. msg por ale6000
-
- 2 Resp.
- 636 Exibições
-
Últ. msg por Argean
-
- 1 Resp.
- 6641 Exibições
-
Últ. msg por VALDECIRTOZZI
-
- 1 Resp.
- 1262 Exibições
-
Últ. msg por Bira
-
- 4 Resp.
- 6381 Exibições
-
Últ. msg por MatheusBorges

