Dados: Massas molares (g/mol): CaCO3 = 100 g/mol; CO = 44 g/mol; HCL = 36,5 g/mol
0 K = 273 ºC e 273 K = 0 ºC
Constante dos gases ideais: R = 0,082 atm.L.mol .K
O cálcário é um minério que apresenta elevado teor de carbonato de cálcio (CaCO3 ) além de outras impurezas.
Uma amostra de 2,00 g de calcário foi tratada com 100 mL de solução aquosa de ácido clorídrico (HCL ) de
concentração 0,50 mol.L . O gás carbônico (CO2) obtido nesse processo foi armazenado em um recipiente de
4,1 L a 27ºC, apresentando pressão parcial de 0,090 atm.
O teor de carbonato de cálcio nessa amostra de calcário é
(A) 50%
(B) 65%
(C) 75%
(D) 90%
(E) 100%
Físico-Química ⇒ (PUC-SP) Estequiometria Tópico resolvido
Moderador: [ Moderadores TTB ]
-
LuddyWyatt

- Mensagens: 27
- Registrado em: 03 Mai 2012, 15:45
- Última visita: 17-10-15
- Agradeceu: 2 vezes
Ago 2014
18
10:10
(PUC-SP) Estequiometria
Editado pela última vez por poti em 18 Ago 2014, 20:49, em um total de 1 vez.
Razão: Alterar Título
Razão: Alterar Título
- VALDECIRTOZZI

- Mensagens: 2569
- Registrado em: 04 Ago 2008, 17:08
- Última visita: 13-10-20
- Agradeceu: 197 vezes
- Agradeceram: 1590 vezes
Ago 2014
19
07:53
Re: (PUC-SP) Estequiometria
A reação química do processo é:
}+ 2 HC\ell_{(aq)} \rightarrow CaC\ell_2_{(aq)}+CO_2_{(g)}+H_2O_{(\ell)})
Utilizando a equação de Clayperon, popdemos calcular o número de mols de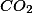 formado:
formado:



Pela estequeometria da reação, 1 mol de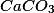 gera 1 mol de
gera 1 mol de 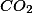 , portanto, reagiram
, portanto, reagiram  .
.




Espero ter ajudado!
Utilizando a equação de Clayperon, popdemos calcular o número de mols de
Pela estequeometria da reação, 1 mol de
Espero ter ajudado!
Editado pela última vez por VALDECIRTOZZI em 19 Ago 2014, 07:53, em um total de 1 vez.
So many problems, so little time!
-
- Tópicos Semelhantes
- Respostas
- Exibições
- Última mensagem
-
- 1 Respostas
- 6120 Exibições
-
Última mensagem por VALDECIRTOZZI
-
- 1 Respostas
- 11666 Exibições
-
Última mensagem por MatheusBorges
-
- 1 Respostas
- 1021 Exibições
-
Última mensagem por Jigsaw
-
- 1 Respostas
- 3075 Exibições
-
Última mensagem por Cientista
-
- 2 Respostas
- 912 Exibições
-
Última mensagem por MicheleAlves
