Olá pessoal, eu queria entender a questão abaixo. Eu conheço as três teorias ácido-base de Arrhenius, Bronsted-Lowry e Lewis.
Porém, não consigo ver na equação abaixo o porquê do HCL ser um ácido de Lewis. Pois, segundo o que estudei, ácido de Lewis é aquele que receber pares de elétron( todos os cátions ou moléculas que não possui o octeto completo ao redor). Com isso, eu não consigo achar uma justificativa para que o HCl seja ácido de Lewis. Poderiam me ajudar? O que estou fazendo de errado? É alguma definição?
A questão é para marcar as alternativas verdadeiras e falsas, e minha dúvida é nessa abaixo que é considerada verdadeira:
* Na reação : HCl(aq) + NaOH(aq) ---> NaCl9aq) + H2O(l), HCl é um ácido e NaOH uma base, segundo Arrhenius, Bronsed-Lowry e Lewis, respectivamente.
Fiquei pensando se estou errando na interpretação da questão também. Espero a ajuda de vocês!
Química Geral ⇒ Reações químicas - Teorias Ácido-Base
Moderador: [ Moderadores TTB ]
-
MariaIsadora

- Mensagens: 6
- Registrado em: 05 Mar 2016, 22:34
- Última visita: 13-07-16
- Agradeceu: 1 vez
-
VALDECIRTOZZI

- Mensagens: 2569
- Registrado em: 04 Ago 2008, 17:08
- Última visita: 13-10-20
- Agradeceu: 197 vezes
- Agradeceram: 1590 vezes
Jun 2016
02
09:02
Re: Reações químicas - Teorias Ácido-Base
Creio que a explicação deve passar pelas seguintes etapas:
Imagine uma molécula de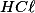 que ao se dissolver em água libera o íon
que ao se dissolver em água libera o íon 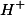 .
.
Esse íon hidrogênio se liga a uma molécula de água vizinha (que dispõe de par de elétrons livres). Nesse caso a água doa o par de elétrons, é uma base de Lewis, e o íon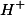 recebe esse par de elétrons, é o ácido de Lewis, formando o íon hidroxônio
recebe esse par de elétrons, é o ácido de Lewis, formando o íon hidroxônio 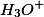 .
.
Espero ter ajudado!
Imagine uma molécula de
Esse íon hidrogênio se liga a uma molécula de água vizinha (que dispõe de par de elétrons livres). Nesse caso a água doa o par de elétrons, é uma base de Lewis, e o íon
Espero ter ajudado!
Editado pela última vez por VALDECIRTOZZI em 02 Jun 2016, 09:02, em um total de 1 vez.
So many problems, so little time!
-
MariaIsadora

- Mensagens: 6
- Registrado em: 05 Mar 2016, 22:34
- Última visita: 13-07-16
- Agradeceu: 1 vez
Jun 2016
02
11:55
Re: Reações químicas - Teorias Ácido-Base
Então, mas se for considerar os íons separados, caso o H+ seja ácido de Lewis, o CL- seria base de Lewis( Todo ânion é base). Então HCL seria o que?VALDECIRTOZZI escreveu:Creio que a explicação deve passar pelas seguintes etapas:
Imagine uma molécula deque ao se dissolver em água libera o íon
.
Esse íon hidrogênio se liga a uma molécula de água vizinha (que dispõe de par de elétrons livres). Nesse caso a água doa o par de elétrons, é uma base de Lewis, e o íonrecebe esse par de elétrons, é o ácido de Lewis, formando o íon hidroxônio
.
Espero ter ajudado!
Editado pela última vez por MariaIsadora em 02 Jun 2016, 11:55, em um total de 1 vez.
-
marcosdrey

- Mensagens: 1
- Registrado em: 06 Jun 2016, 15:29
- Última visita: 07-06-16
Jun 2016
06
16:37
Re: Reações químicas
Boa tarde,
Gostaria de tirar uma duvida sobre os produtos Lustra Movies e Detergente, pois misturando ambos, sua solução facilita na remoção de manchas como "mancha de Óleo" sobre tecidos.
Alguém poderia me esclarecer porque isso acontece?
Gostaria de tirar uma duvida sobre os produtos Lustra Movies e Detergente, pois misturando ambos, sua solução facilita na remoção de manchas como "mancha de Óleo" sobre tecidos.
Alguém poderia me esclarecer porque isso acontece?
-
- Tópicos Semelhantes
- Respostas
- Exibições
- Última mensagem
-
- 1 Respostas
- 1166 Exibições
-
Última mensagem por A13235378
-
- 1 Respostas
- 660 Exibições
-
Última mensagem por VALDECIRTOZZI
-
- 4 Respostas
- 4305 Exibições
-
Última mensagem por GabrielaC
-
- 1 Respostas
- 7158 Exibições
-
Última mensagem por VALDECIRTOZZI
-
- 2 Respostas
- 825 Exibições
-
Última mensagem por guilhermeP
