FISMAQUIM, primeiro indicamos a distribuição eletrônica:
De acordo com a distribuição eletrônica do I:
[tex3]I : 1s^2\ 2s^2\ 2p^6\ 3s^2\ 3p^6\ 4s^2\ 3d^10\ 4p^6\ 5s^2\ 4d^{10}\ 5p^5[/tex3]
[tex3]I : K = 2\ L = 8\ M = 18\ N = 18\ O = 7[/tex3]
Observando a configuração mais energética temos:
[tex3]\boxed{\uparrow \downarrow}\hspace{0,2cm}\boxed{\uparrow \downarrow}\boxed{\uparrow \downarrow}\boxed{\uparrow\ }[/tex3]
5s2 [tex3]\hspace{1,0cm}[/tex3]
5p5
Procedendo com a hibridização dos orbitais:
[tex3]\boxed{\uparrow \downarrow}\hspace{0,2cm}\boxed{\uparrow\ }\boxed{\uparrow\ }\boxed{\uparrow\ }\hspace{0,2cm}\boxed{\uparrow\ }\boxed{\uparrow\ }[/tex3]
5s2 [tex3]\hspace{1,3cm}[/tex3]
5p3 [tex3]\hspace{1,7cm}[/tex3]
5d2
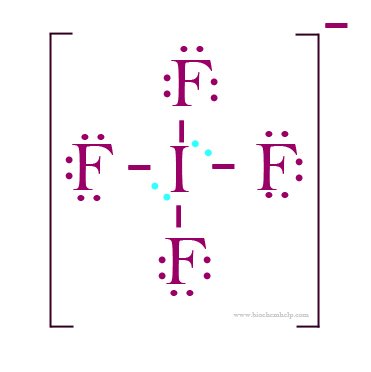
- p5EvHO6tRqyMkqFt2q0C_IF4ion-lewisstructure.jpg (10.92 KiB) Exibido 1408 vezes
Fórmula = AX4E2
geometria = quadrado planar
hibridização = sp3d2
maior ângulo = 90 º
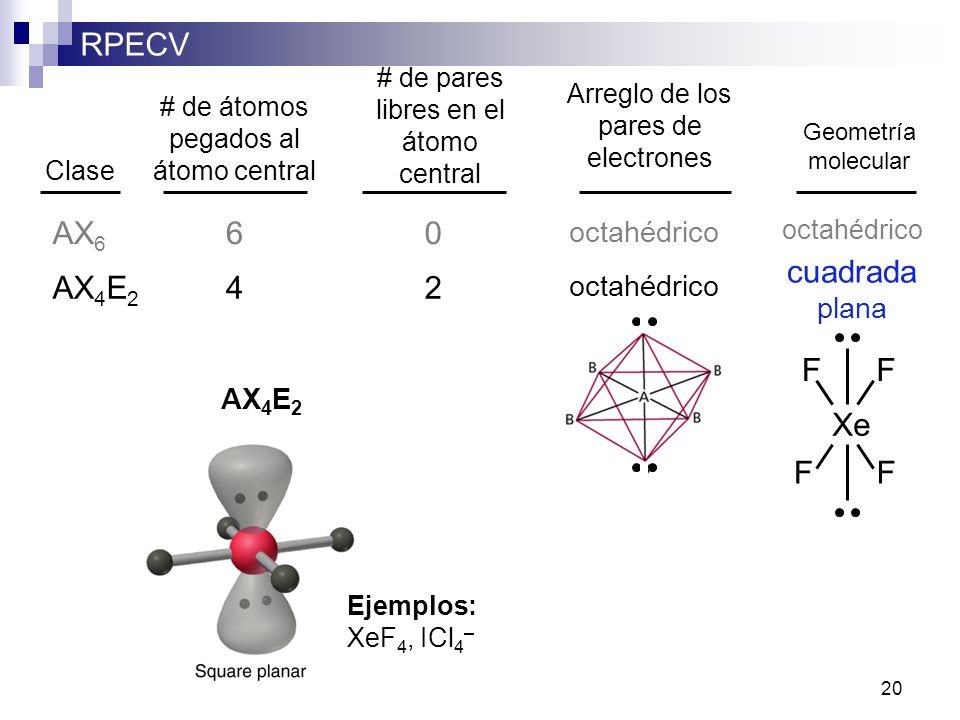
- AX4E2.jpg (62.38 KiB) Exibido 1399 vezes
Note que a geometria do IF4- é semelhante a do ICl4- (quadrado planar) o ângulo de 90º refere-se as ligações I - F, no caso dos eletrons desemparelhados o ângulo de ligação é de 180º portanto a alternativa correta é a D.

