Página 1 de 1
(ITA) Titulação
Enviado: 08 Out 2014, 12:32
por leopbi22
Uma placa constituída por uma liga de estanho foi pesada e apresentou 500 mg foi solubilizada e o estanho presente reduzido completamente a estanho II por níquel metálico. Para a determinação do teor de estanho, foi feita uma titulação com 42 ml de uma solução 0,1 N de iodo. Calcule a porcentagem de estanho na liga metálica analisada.
Re: (ITA) Titulação
Enviado: 08 Out 2014, 15:25
por VALDECIRTOZZI
A reação envolvida na titulação é:
}+I_2_{(aq)}\rightarrow Sn^{4+}_{(aq)}+2I^-_{(aq)})
O número de equivalente de

é:
=0,1 \cdot 0,042=0,0042 \equivalentes)
Como na reação sempre 1 equivalente reage com 1 equivalente, o

Temos ainda que:

em que
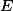
é o equivalente-grama.
O

na reação em questão é a

, já que 1 mol de estanho liberam 2 elétrons.

Daí:




Espero ter ajudado!
Re: (ITA) Titulação
Enviado: 08 Out 2014, 16:15
por leopbi22
Amigo, acho que vc esqueceu de passar 500mg para grama , ou estou errado?
Obrigado pela ajuda.
Re: (ITA) Titulação
Enviado: 10 Out 2014, 07:51
por VALDECIRTOZZI
Note que a massa de estanho que eu achei está em gramas na parte final do cálculo.