Um grande condomínio utiliza como fonte de energia elétrica a queima de um combustível gasoso na vazão de 5 x [tex3]10^{3}[/tex3]
L.h. A região do condominio pode ser abastecida por quatro combustíveis gasosos encanados. Suas composições, em volume, são demonstradas na tabela abaixo.
I - gás natural leve: 90% metano - 10% etano
II - gás natural pesado: 80% metano - 20% etano
III - gás liquefeito leve: 80% butano - 20% propano
IV - gas liquefeito pesado: 90% butano - 10% propano
O combustível gasoso utilizado pelo condomínio, sabendo que sua combustão completa libera 1,32 x [tex3]10^{5}[/tex3]
L de gás carbônico por dia, sob pressão e temperatura constantes, é o de número:
a) I
b) II
c) III
d) IV
Res.: A
Físico-Química ⇒ Combustão completa Tópico resolvido
- izabelaalves

- Mensagens: 16
- Registrado em: 10 Mai 2015, 22:26
- Última visita: 24-06-15
- Agradeceu: 9 vezes
Mai 2015
28
20:03
Combustão completa
Editado pela última vez por izabelaalves em 28 Mai 2015, 20:03, em um total de 1 vez.
- VALDECIRTOZZI

- Mensagens: 2569
- Registrado em: 04 Ago 2008, 17:08
- Última visita: 13-10-20
- Agradeceu: 197 vezes
- Agradeceram: 1590 vezes
Mai 2015
29
07:32
Re: Combustão completa
O fornecimento de gás diário é: 
Caso I:


Observando a estequiometria das reações:
Sendo , o volume fornecido de
, o volume fornecido de  , obteremos a formação de
, obteremos a formação de  de
de 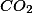 .
.
Sendo , o volume fornecido de
, o volume fornecido de  , obteremos a formação de
, obteremos a formação de  de
de 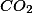 .
.
Com essas informações, podemos montar o sistema:

Resolvendo o sistema,temos:


Então:


Note que esse resultado invalida II.
Caso III:


Observando a estequiometria das reações:
Sendo , o volume fornecido de
, o volume fornecido de  , obteremos a formação de
, obteremos a formação de  de
de 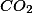 .
.
Sendo , o volume fornecido de
, o volume fornecido de  , obteremos a formação de
, obteremos a formação de  de
de 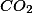 .
.
Com essas informações, podemos montar o sistema:

Resolvendo o sistema,temos:


Pelos resultados, vemos que é impossível qualquer proporção com esses dois gases.
Espero ter ajudado!
Caso I:
Observando a estequiometria das reações:
Sendo
Sendo
Com essas informações, podemos montar o sistema:
Resolvendo o sistema,temos:
Então:
Note que esse resultado invalida II.
Caso III:
Observando a estequiometria das reações:
Sendo
Sendo
Com essas informações, podemos montar o sistema:
Resolvendo o sistema,temos:
Pelos resultados, vemos que é impossível qualquer proporção com esses dois gases.
Espero ter ajudado!
Editado pela última vez por VALDECIRTOZZI em 29 Mai 2015, 07:32, em um total de 1 vez.
So many problems, so little time!
-
- Tópicos Semelhantes
- Resp.
- Exibições
- Últ. msg
-
- 2 Resp.
- 1370 Exibições
-
Últ. msg por Jigsaw
-
- 0 Resp.
- 232 Exibições
-
Últ. msg por Hudson535
-
- 2 Resp.
- 1053 Exibições
-
Últ. msg por TarekVilela
-
- 1 Resp.
- 416 Exibições
-
Últ. msg por ttbr96
-
- 1 Resp.
- 616 Exibições
-
Últ. msg por ttbr96
