Suponha uma volumetria entre 100,00 mL de uma solução de Ácido Acético (CH3COOH) de concentração 0,100 mol L-1, com NaOH 0,100 mol L-1. Calcule o pH da solução quando é adicionado: (considere Kaac.acetico = 1,8 x 10-5)
a. Qual o pH da solução quando se adiciona 10 mL de NaOH?
b. Qual o pH no ponto de equivalência?
c. Qual o volume de NaOH que é adicionado para se obter a capacidade tamponante máxima?
Físico-Química ⇒ UFG 2013/1 - pH e equilibrio quimico
Moderador: [ Moderadores TTB ]
- VALDECIRTOZZI

- Mensagens: 2569
- Registrado em: 04 Ago 2008, 17:08
- Última visita: 13-10-20
- Agradeceu: 197 vezes
- Agradeceram: 1590 vezes
Mar 2015
24
08:50
Re: UFG 2013/1 - pH e equilibrio quimico
A reação entre ácido fraco, ácido acético ) e a base forte, hidróxido de sódio
e a base forte, hidróxido de sódio ) , pode ser assim escrita:
, pode ser assim escrita:
}+NaOH_{(aq)} \leftrightharpoons NaAc_{(aq)}+H_2O_{(\ell)})
a) Quando se adicionam 10 mL de base, há formação de acetato de sódio aquoso e permanece, em solução, o ácido acético que não foi neutralizado, formando um tampão.
Como a estequiometria da reação é 1 : 1 temos:
![\left[HAc\right]=\frac{100 \times 0,1-10 \times 0,1}{110}=0,08182 \ mol/\ell \left[HAc\right]=\frac{100 \times 0,1-10 \times 0,1}{110}=0,08182 \ mol/\ell](https://www.tutorbrasil.com.br/latex/mathtex.cgi?\left[HAc\right]=\frac{100 \times 0,1-10 \times 0,1}{110}=0,08182 \ mol/\ell)
![\left[NaAc\right]=\frac{10 \times 0,1}{110}=0,009091 \ mol/\ell \left[NaAc\right]=\frac{10 \times 0,1}{110}=0,009091 \ mol/\ell](https://www.tutorbrasil.com.br/latex/mathtex.cgi?\left[NaAc\right]=\frac{10 \times 0,1}{110}=0,009091 \ mol/\ell)
A ionização do ácido acético é representada por:
} \leftrightharpoons H^+_{(aq)}+Ac_{(aq)}^-)
![k_a=\frac{\left[Ac^-\right]\cdot \left[H^+\right]}{\left[HAc\right]} k_a=\frac{\left[Ac^-\right]\cdot \left[H^+\right]}{\left[HAc\right]}](https://www.tutorbrasil.com.br/latex/mathtex.cgi?k_a=\frac{\left[Ac^-\right]\cdot \left[H^+\right]}{\left[HAc\right]})
![1,8 \times 10^{-5}=\frac{0,009091 \cdot \left[H^+\right]}{0,08182} 1,8 \times 10^{-5}=\frac{0,009091 \cdot \left[H^+\right]}{0,08182}](https://www.tutorbrasil.com.br/latex/mathtex.cgi?1,8 \times 10^{-5}=\frac{0,009091 \cdot \left[H^+\right]}{0,08182})
![\left[H^+\right]=1,62 \times 10^{-4} \ mol/\ell \left[H^+\right]=1,62 \times 10^{-4} \ mol/\ell](https://www.tutorbrasil.com.br/latex/mathtex.cgi?\left[H^+\right]=1,62 \times 10^{-4} \ mol/\ell)

b) No ponto de equivalência, todo ácido acético foi convertido em acetato de sódio, e o pH será dado pela hidrólise do sal.
}^-+H_2O_{(\ell)} \leftrightharpoons HAc_{(aq)}+OH_{(aq)}^-)
![k_h=\frac{\left[HAc\right] \cdot \left[OH^-\right]}{\left[Ac^-]} k_h=\frac{\left[HAc\right] \cdot \left[OH^-\right]}{\left[Ac^-]}](https://www.tutorbrasil.com.br/latex/mathtex.cgi?k_h=\frac{\left[HAc\right] \cdot \left[OH^-\right]}{\left[Ac^-]})
Note que:![\left[HAc\right]=\left[OH^-\right] \left[HAc\right]=\left[OH^-\right]](https://www.tutorbrasil.com.br/latex/mathtex.cgi?\left[HAc\right]=\left[OH^-\right])
E ainda: para neutralizar todo acético) , é necessário 0,01 mol de base. Como a concentração da base é 0,1 mol/L, são necessários 100 mL dela. O volume no ponto de equivalência é 200 mL. Daí titamos que a
, é necessário 0,01 mol de base. Como a concentração da base é 0,1 mol/L, são necessários 100 mL dela. O volume no ponto de equivalência é 200 mL. Daí titamos que a ![\left[Ac^-\right] \left[Ac^-\right]](https://www.tutorbrasil.com.br/latex/mathtex.cgi?\left[Ac^-\right]) será:
será:
![\left[Ac^-\right]=\frac{100 \cdot 0,1}{200}=0,05 \ mol/\ell \left[Ac^-\right]=\frac{100 \cdot 0,1}{200}=0,05 \ mol/\ell](https://www.tutorbrasil.com.br/latex/mathtex.cgi?\left[Ac^-\right]=\frac{100 \cdot 0,1}{200}=0,05 \ mol/\ell)
![k_h=\frac{\left[HAc\right] \cdot \left[OH^-\right]}{\left[Ac^-]} k_h=\frac{\left[HAc\right] \cdot \left[OH^-\right]}{\left[Ac^-]}](https://www.tutorbrasil.com.br/latex/mathtex.cgi?k_h=\frac{\left[HAc\right] \cdot \left[OH^-\right]}{\left[Ac^-]})
![\frac{k_w}{k_a}=\frac{\left[HAc\right] \cdot \left[OH^-\right]}{\left[Ac^-]} \frac{k_w}{k_a}=\frac{\left[HAc\right] \cdot \left[OH^-\right]}{\left[Ac^-]}](https://www.tutorbrasil.com.br/latex/mathtex.cgi?\frac{k_w}{k_a}=\frac{\left[HAc\right] \cdot \left[OH^-\right]}{\left[Ac^-]})
![\frac{10^{-14}}{1,8 \times 10^{-5}}=\frac{\left[HAc\right] \cdot \left[OH^-\right]}{\left[Ac^-]} \frac{10^{-14}}{1,8 \times 10^{-5}}=\frac{\left[HAc\right] \cdot \left[OH^-\right]}{\left[Ac^-]}](https://www.tutorbrasil.com.br/latex/mathtex.cgi?\frac{10^{-14}}{1,8 \times 10^{-5}}=\frac{\left[HAc\right] \cdot \left[OH^-\right]}{\left[Ac^-]})
Como é muito pequena, podemos considerar que
é muito pequena, podemos considerar que ![\left[Ac^-\right] \left[Ac^-\right]](https://www.tutorbrasil.com.br/latex/mathtex.cgi?\left[Ac^-\right]) final, após a hidrólise é praticamente 0,05 mol/L.
final, após a hidrólise é praticamente 0,05 mol/L.
![5,55 \times 10^{-10}=\frac{\left[OH^-\right]^2}{0,05} 5,55 \times 10^{-10}=\frac{\left[OH^-\right]^2}{0,05}](https://www.tutorbrasil.com.br/latex/mathtex.cgi?5,55 \times 10^{-10}=\frac{\left[OH^-\right]^2}{0,05})
![\left[OH^-\right]=5,27 \times 10^{-6} \ mol/\ell \left[OH^-\right]=5,27 \times 10^{-6} \ mol/\ell](https://www.tutorbrasil.com.br/latex/mathtex.cgi?\left[OH^-\right]=5,27 \times 10^{-6} \ mol/\ell)


c) O pH do tampão é dado por:
![pH=pk_a+\log \frac{\left[Ac^-\right]}{\left[HAc\right]} pH=pk_a+\log \frac{\left[Ac^-\right]}{\left[HAc\right]}](https://www.tutorbrasil.com.br/latex/mathtex.cgi?pH=pk_a+\log \frac{\left[Ac^-\right]}{\left[HAc\right]})
A capacidade máxima do tampão ocorre quando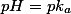 , ou
, ou ![\log \frac{\left[Ac^-\right]}{\log \left[HAc\right]}=0 \log \frac{\left[Ac^-\right]}{\log \left[HAc\right]}=0](https://www.tutorbrasil.com.br/latex/mathtex.cgi?\log \frac{\left[Ac^-\right]}{\log \left[HAc\right]}=0) ou
ou ![\frac{\left[Ac^-\right]}{\left[HAc\right]}=1 \frac{\left[Ac^-\right]}{\left[HAc\right]}=1](https://www.tutorbrasil.com.br/latex/mathtex.cgi?\frac{\left[Ac^-\right]}{\left[HAc\right]}=1)
Para que![\left[Ac^-\right]=\left[HAc\right] \left[Ac^-\right]=\left[HAc\right]](https://www.tutorbrasil.com.br/latex/mathtex.cgi?\left[Ac^-\right]=\left[HAc\right]) , teremos que ter a metade da quantidade inicial de ácido acético convertida em acetato de sódio.
, teremos que ter a metade da quantidade inicial de ácido acético convertida em acetato de sódio.
A quantidade inicial de ácido acético é 0,01 mol. Deve então restar, em solução, 0,005 mol do ácido e, para tanto, o ácido deve ser neutralizado com 0,05 mol de base. Como a concentração de base é 0,1 mol/L, deve-se ser adicionado 0,05 L ou 50 mL de base.
Espero ter ajudado!
a) Quando se adicionam 10 mL de base, há formação de acetato de sódio aquoso e permanece, em solução, o ácido acético que não foi neutralizado, formando um tampão.
Como a estequiometria da reação é 1 : 1 temos:
A ionização do ácido acético é representada por:
b) No ponto de equivalência, todo ácido acético foi convertido em acetato de sódio, e o pH será dado pela hidrólise do sal.
Note que:
E ainda: para neutralizar todo acético
Como
c) O pH do tampão é dado por:
A capacidade máxima do tampão ocorre quando
Para que
A quantidade inicial de ácido acético é 0,01 mol. Deve então restar, em solução, 0,005 mol do ácido e, para tanto, o ácido deve ser neutralizado com 0,05 mol de base. Como a concentração de base é 0,1 mol/L, deve-se ser adicionado 0,05 L ou 50 mL de base.
Espero ter ajudado!
Editado pela última vez por VALDECIRTOZZI em 24 Mar 2015, 08:50, em um total de 1 vez.
So many problems, so little time!
-
- Tópicos Semelhantes
- Respostas
- Exibições
- Última mensagem
-
- 2 Respostas
- 30030 Exibições
-
Última mensagem por anagiulial
-
- 4 Respostas
- 1489 Exibições
-
Última mensagem por Jigsaw
-
- 1 Respostas
- 1299 Exibições
-
Última mensagem por VALDECIRTOZZI
-
- 2 Respostas
- 3401 Exibições
-
Última mensagem por csmarcelo
-
- 6 Respostas
- 3830 Exibições
-
Última mensagem por Andre13000

