A equação química que representa o processo é:
}+2 \ NaOH \rightarrow Na_2SO_4_{(aq)}+2 H_2O_{(\ell)})
Note que 1 mol de

reagem com 2 mols de

.
Lembre-se de que:
})
, onde:

é a concentração molar do soluto;

é o número de mols do soluto;
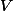
é o volume, em litros, da solução.
Para o

:
})


Para o

:
})


Como a proporção molar é 1 mol de ácido para 2 mols de base, podemos concluir que 0,04 mols de base necessitam de 0,02 mol de ácido, sendo o ácido o regente em excesso.
(Note que se fizesse o seguinte raciocínio: 0,04 mol de ácido precisaria de 0,08 mols de base e essa quantidade não está disponível, concluiria, da mesma forma, que o ácido é o reagente em excesso)
Ora se há 0,04 mol de ácido e foi consumido, na reação com a base, 0,02 de ácido sobra, em solução, 0,02 mol de ácido. O volume da solução, após a reação é de 400 mL;
})


Espero ter ajudado!


