A 25ºC e pressão de 1 atm, a queima completa de um mol de n-hexano produz dióxido de carbono
e água no estado gasoso e libera 3883 kJ, enquanto que a queima completa da mesma quantidade
de n-heptano produz as mesmas substâncias no estado gasoso e libera 4498 kJ.
a) Utilizando as informações fornecidas no enunciado desta questão, faça uma estimativa do valor
do calor de combustão do n-decano. Deixe claro o raciocínio utilizado na estimativa realizada.
IME/ITA ⇒ (ITA 2001) Termoquímica Tópico resolvido
Moderador: [ Moderadores TTB ]
-
VALDECIRTOZZI

- Mensagens: 2569
- Registrado em: Seg 04 Ago, 2008 17:08
- Última visita: 13-10-20
Dez 2012
17
15:52
Re: (ITA 2001) Termoquímica
Creio que o raciocínio a ser utilizado aqui é sobre energias de ligação. Considere as reações de combustão:
%7D%20+%5Cfrac%7B19%7D%7B2%7DO_2_%7B(g)%7D%20%5Crightarrow%206CO_2_%7B(g)%7D+7H_2O_%7B(g)%7D)
%7D%20+11O_2_%7B(g)%7D%20%5Crightarrow%207CO_2_%7B(g)%7D+8H_2O_%7B(g)%7D)
%7D%20+%5Cfrac%7B31%7D%7B2%7DO_2_%7B(g)%7D%20%5Crightarrow%2010CO_2_%7B(g)%7D+11H_2O_%7B(g)%7D)
No n-hexano: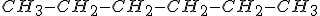 , temos o rompimento de 5 mols de ligações
, temos o rompimento de 5 mols de ligações 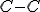 e 14 mols de ligação
e 14 mols de ligação 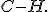
No n-heptano: , temos o rompimento de 7 mols de ligação
, temos o rompimento de 7 mols de ligação 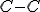 e 16 mols de ligação
e 16 mols de ligação 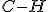 .
.
Há ainda, 9,5 mols de ligação na combustão do n-hexano rompidas, enquanto que na combustão do n-heptano se rompem 11 mols dessa ligação.
na combustão do n-hexano rompidas, enquanto que na combustão do n-heptano se rompem 11 mols dessa ligação.
Quanto aos produtos temos que no n-hexano se formam 12 mols de ligação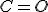 e 14 mols de ligações
e 14 mols de ligações 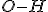 .
.
No n-heptano se formam 14 mols de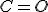 ligações e 16 mols de ligações
ligações e 16 mols de ligações 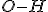 .
.
Tudo isso faz com que a combustão do n-hexano libere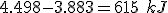 de energia mais.
de energia mais.
Agora, o n-decano há quebra de 10 mols de ligações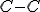 , 22 mols de ligações
, 22 mols de ligações 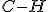 , 15,5 mols de ligações
, 15,5 mols de ligações  . Há formação de 20 mols de ligações
. Há formação de 20 mols de ligações 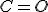 e 22 mols de ligações
e 22 mols de ligações 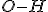 .
.
Olhando essas conclusões, vemos que no n-decano se rompem a mais que o n-heptano (em mols): 3 ligações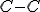 ; 6 ligações
; 6 ligações 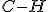 , 4,5 ligações
, 4,5 ligações  .
.
Formam-se a mais que no n-heptano (em mols): 6 ligações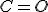 e 6 ligações
e 6 ligações 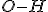 .
.
Ora, isso é o triplo do número de rompimento/formação do n-heptano em relação ao n-hexano. Então:
![\Delta H=[-4.498+3(-615)]=-6.346 \ kJ \Delta H=[-4.498+3(-615)]=-6.346 \ kJ](https://www.tutorbrasil.com.br/latex/mimetex_.cgi?%5CDelta%20H=%5B-4.498+3(-615)%5D=-6.346%20%5C%20kJ)
Espero ter ajudado!
No n-hexano:
No n-heptano:
Há ainda, 9,5 mols de ligação
Quanto aos produtos temos que no n-hexano se formam 12 mols de ligação
No n-heptano se formam 14 mols de
Tudo isso faz com que a combustão do n-hexano libere
Agora, o n-decano há quebra de 10 mols de ligações
Olhando essas conclusões, vemos que no n-decano se rompem a mais que o n-heptano (em mols): 3 ligações
Formam-se a mais que no n-heptano (em mols): 6 ligações
Ora, isso é o triplo do número de rompimento/formação do n-heptano em relação ao n-hexano. Então:
Espero ter ajudado!
Última edição: VALDECIRTOZZI (Seg 17 Dez, 2012 15:52). Total de 1 vez.
So many problems, so little time!
-
- Tópicos Semelhantes
- Respostas
- Exibições
- Última msg
-
- 1 Respostas
- 1792 Exibições
-
Última msg por Jigsaw
-
- 0 Respostas
- 541 Exibições
-
Última msg por iammaribrg
-
- 0 Respostas
- 550 Exibições
-
Última msg por LadyGodiva
-
- 1 Respostas
- 1529 Exibições
-
Última msg por Ósmio
-
- 0 Respostas
- 451 Exibições
-
Última msg por iammaribrg








