Um reservatório fechado contém certa quantidade de hélio gasoso à pressão [tex3]\rho_i.[/tex3]
Num primeiro processo, esse gás é aquecido, lentamente, de uma temperatura inicial [tex3]T_i[/tex3]
até uma temperatura [tex3]T_F.[/tex3]
Num segundo processo, um pequeno orifício é aberto na parede do reservatório e, por ele, muito lentamente, deixa-se escapar um quarto do conteúdo inicial do gás. Durante esse processo, o reservatório é mantido à temperatura [tex3]T_F.[/tex3]
Considerando essas informações,
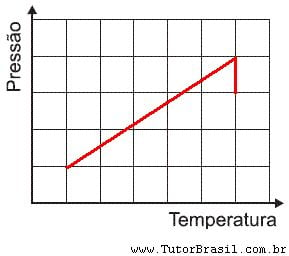
1. ESBOCE, no quadro ao abaixo, o diagrama da pressão em função da temperatura do gás nos dois processos descritos.
JUSTIFIQUE sua resposta. (eu acho que até conseguiria fazer o grafico usando um pouco de lógica, o problema seria pra justificar..=/ )
2. Considere que [tex3]\rho_i = 1,0 \times10^5\, \text{N/m^2}[/tex3]
e que as temperaturas são [tex3]T_i = 27^\circ \text{C}[/tex3]
e [tex3]T_F = 87^\circ \text{C}.[/tex3]
CALCULE o valor da pressão do gás no interior do reservatório, ao final do segundo processo.
Física II ⇒ (UFMG - 2007) Pressão
- LucasMattos

- Mensagens: 16
- Registrado em: 06 Out 2007, 13:52
- Última visita: 07-11-07
- Agradeceram: 1 vez
Out 2007
20
10:02
(UFMG - 2007) Pressão
Editado pela última vez por LucasMattos em 20 Out 2007, 10:02, em um total de 2 vezes.
- Alexandre_SC

- Mensagens: 505
- Registrado em: 06 Mai 2007, 21:13
- Última visita: 28-06-11
- Localização: Joinville - SC
- Agradeceram: 11 vezes
Out 2007
21
22:57
Re: (UFMG - 2007) Pressão
no primeiro o gráfico é uma reta inclinada
pois o volume é constante e a quantidade de gas é constante
então aplicando aquele fórmula
[tex3]pV = nRT[/tex3]
[tex3]p = \frac{nR}{V}\cdot T[/tex3]
então essa reta parte de
[tex3]\frac{nRT_i}{V}[/tex3]
e termina em [tex3]\frac{NRT_F}{V}[/tex3]
e no segundo processo a pressão varia enquanto a temperatura se mantem constante
a pressão começa em
[tex3]\frac{nRT_F}{V}[/tex3]
mas tres quartos do gás sai
ficando com uma pressão de [tex3]\frac{n}{4} \cdot \frac{RT_F}{V}[/tex3]
temos que a pressão inicial é de
[tex3]10^5N/m^2[/tex3] ? se for 105 mesmo é só substituir o valor
e Ti = 27°C = 300°K
então podemos encontrar a quantidade de gás
[tex3]pV = nRT\Right m = \frac{pV}{RT}[/tex3]
[tex3]n = \frac{10^5V}{R\cdot 300}[/tex3]
como já havia dito
a pressão final é dada por
[tex3]\frac{nRT_F}{V}[/tex3]
[tex3]T_F[/tex3] = 87° C = 360°K
substituindo a expressão acima temos
[tex3]\frac{\left( \frac{10^5\cancel V}{R\cdot 300}\right)R\cdot 360}{ \cancel V}[/tex3]
[tex3]\left( \frac{10^5}{\cancel R\cdot 300}\right)\cancel R\cdot 360[/tex3]
[tex3]\frac{10^5\cdot 360}{R\cdot 300} = \frac{6}{5}\cdot 10^5 = 12\cdot 10^4[/tex3]
[tex3]12\cdot 10^4 N/m^2[/tex3]
pois o volume é constante e a quantidade de gas é constante
então aplicando aquele fórmula
[tex3]pV = nRT[/tex3]
[tex3]p = \frac{nR}{V}\cdot T[/tex3]
então essa reta parte de
[tex3]\frac{nRT_i}{V}[/tex3]
e termina em [tex3]\frac{NRT_F}{V}[/tex3]
e no segundo processo a pressão varia enquanto a temperatura se mantem constante
a pressão começa em
[tex3]\frac{nRT_F}{V}[/tex3]
mas tres quartos do gás sai
ficando com uma pressão de [tex3]\frac{n}{4} \cdot \frac{RT_F}{V}[/tex3]
temos que a pressão inicial é de
[tex3]10^5N/m^2[/tex3] ? se for 105 mesmo é só substituir o valor
e Ti = 27°C = 300°K
então podemos encontrar a quantidade de gás
[tex3]pV = nRT\Right m = \frac{pV}{RT}[/tex3]
[tex3]n = \frac{10^5V}{R\cdot 300}[/tex3]
como já havia dito
a pressão final é dada por
[tex3]\frac{nRT_F}{V}[/tex3]
[tex3]T_F[/tex3] = 87° C = 360°K
substituindo a expressão acima temos
[tex3]\frac{\left( \frac{10^5\cancel V}{R\cdot 300}\right)R\cdot 360}{ \cancel V}[/tex3]
[tex3]\left( \frac{10^5}{\cancel R\cdot 300}\right)\cancel R\cdot 360[/tex3]
[tex3]\frac{10^5\cdot 360}{R\cdot 300} = \frac{6}{5}\cdot 10^5 = 12\cdot 10^4[/tex3]
[tex3]12\cdot 10^4 N/m^2[/tex3]
Editado pela última vez por Alexandre_SC em 21 Out 2007, 22:57, em um total de 1 vez.
Se você não pode ajudar, atrapalhe, porque o importante é participar!
- LucasMattos

- Mensagens: 16
- Registrado em: 06 Out 2007, 13:52
- Última visita: 07-11-07
- Agradeceram: 1 vez
Out 2007
24
20:27
Re: (UFMG - 2007) Pressão
Ih, foi mal, o 105 tava errado mesmo... eh isso mesmo que vc fez..
só ali quando vc disse que 3/4 saem, na verdade 3/4 ficam... então seria 3n/4
só pra conferir o gráfico
uma duvida: no gráfico, a pressão cai exatamente 1/4? ja que é 1/4 do volume que sai e o resto todo se mantém constante?
seria assim?
só ali quando vc disse que 3/4 saem, na verdade 3/4 ficam... então seria 3n/4
só pra conferir o gráfico
uma duvida: no gráfico, a pressão cai exatamente 1/4? ja que é 1/4 do volume que sai e o resto todo se mantém constante?
seria assim?

Editado pela última vez por LucasMattos em 24 Out 2007, 20:27, em um total de 1 vez.
-
- Tópicos Semelhantes
- Resp.
- Exibições
- Últ. msg
-
- 2 Resp.
- 2500 Exibições
-
Últ. msg por Liliana
-
- 7 Resp.
- 1999 Exibições
-
Últ. msg por FelipeMartin
-
- 2 Resp.
- 1896 Exibições
-
Últ. msg por carlosaugusto
-
- 1 Resp.
- 10816 Exibições
-
Últ. msg por MicheleAlves
-
- 1 Resp.
- 3264 Exibições
-
Últ. msg por VALDECIRTOZZI
