Química Geral ⇒ Equilíbrio Químico
Moderador: [ Moderadores TTB ]
-
Cientista

- Mensagens: 1517
- Registrado em: Ter 19 Mar, 2013 16:23
- Última visita: 14-04-17
- Localização: Moçambique-Maputo
- Contato:
Jun 2016
28
11:52
Equilíbrio Químico
Considere o equilíbrio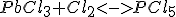 : como seria afectado a posição de equilíbrio:
: como seria afectado a posição de equilíbrio:
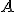) Pela adição de
Pela adição de 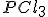 ?
?
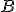) Pela remoção de
Pela remoção de  ?
?
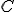) Pela remoção de
Pela remoção de 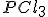 ?
?
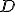) Pela diminuição do volume do recipiente?
Pela diminuição do volume do recipiente?
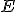) Pela adição de
Pela adição de 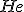 , sem variação de volume?
, sem variação de volume?
Última edição: Cientista (Ter 28 Jun, 2016 11:52). Total de 1 vez.
Força e bons estudos!
-
VALDECIRTOZZI

- Mensagens: 2569
- Registrado em: Seg 04 Ago, 2008 17:08
- Última visita: 13-10-20
Jun 2016
28
12:44
Re: Equilíbrio Químico
veja o sistema está em equilíbrio, ou seja, a velocidade de formação de reação dos reagentes para formar o produto é igual à velocidade de decomposição do produto para formar os reagentes.
Qual "mexida" nesse equilíbrio, o sistema reage tentando restabelecer o equilíbrio, aqui entra o Princípio de le Chatelier
A) A adição de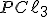 , aumenta sua concentração, então o sistema reage, consumindo mais
, aumenta sua concentração, então o sistema reage, consumindo mais 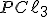 e deslocando a reação para a direita (formação de
e deslocando a reação para a direita (formação de 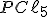 ).
).
B) A remoção de , diminui sua concentração, então o sistema reage, para aumentar sua concentração e se desloca para a esquerda, consumindo mais
, diminui sua concentração, então o sistema reage, para aumentar sua concentração e se desloca para a esquerda, consumindo mais 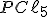 .
.
C) O mesmo efeito acima.
D) Veja que o sistema acima tem 2 volumes de gases na esquerda e 1 volume de gás à direita. Se eu diminuo o volume, há menos espaço para as moléculas, o sistema tenta compensar isso indo para o lado onde o volume é menor, ou seja, para a direita.
E) A introdução de um gás inerte que não reage com os gases presentes no sistema, não afeta o equilíbrio, pois o volumes parciais e pressões parciais dos gases reacionais não se alteram.
Espero ter ajudado!
Qual "mexida" nesse equilíbrio, o sistema reage tentando restabelecer o equilíbrio, aqui entra o Princípio de le Chatelier
A) A adição de
B) A remoção de
C) O mesmo efeito acima.
D) Veja que o sistema acima tem 2 volumes de gases na esquerda e 1 volume de gás à direita. Se eu diminuo o volume, há menos espaço para as moléculas, o sistema tenta compensar isso indo para o lado onde o volume é menor, ou seja, para a direita.
E) A introdução de um gás inerte que não reage com os gases presentes no sistema, não afeta o equilíbrio, pois o volumes parciais e pressões parciais dos gases reacionais não se alteram.
Espero ter ajudado!
Última edição: VALDECIRTOZZI (Ter 28 Jun, 2016 12:44). Total de 1 vez.
So many problems, so little time!
-
- Tópicos Semelhantes
- Respostas
- Exibições
- Última msg
-
- 1 Respostas
- 862 Exibições
-
Última msg por Ósmio
-
- 1 Respostas
- 724 Exibições
-
Última msg por Ósmio
-
- 1 Respostas
- 832 Exibições
-
Última msg por Ósmio
-
- 2 Respostas
- 965 Exibições
-
Última msg por Ósmio
-
- 0 Respostas
- 1199 Exibições
-
Última msg por anastacialina







