Um composto CxH2yOy sofre combustão com um volume de O2 igual a três vezes a quantidade estequiométrica. O sistema gasoso final apresenta volume igual a 7,5 L nas CNTP e a massa de água obtida é igual a 2,0 g. calcule a fórmula molecular do composto CxH2yOy, sabendo que sua massa molecular é igual a 180 u.
R: C6H12O6
Química Orgânica ⇒ Análise Elementar Tópico resolvido
- VALDECIRTOZZI

- Mensagens: 2569
- Registrado em: 04 Ago 2008, 17:08
- Última visita: 13-10-20
- Agradeceu: 197 vezes
- Agradeceram: 1590 vezes
Fev 2015
27
11:42
Re: Análise Elementar
A equação química do processo é:

A quantidade necessário de gás oxigênio é mols, como usei o triplo disso, usei
mols, como usei o triplo disso, usei  . Se reagiram
. Se reagiram  mols, sobraram
mols, sobraram  mols.
mols.







Dividindo pelo menor:
 , cuja massa molar é 30 g/mol
, cuja massa molar é 30 g/mol
Multiplicando por 6:
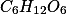
Espero ter ajudado!
A quantidade necessário de gás oxigênio é
Dividindo pelo menor:
Multiplicando por 6:
Espero ter ajudado!
Editado pela última vez por VALDECIRTOZZI em 27 Fev 2015, 11:42, em um total de 1 vez.
So many problems, so little time!
-
- Tópicos Semelhantes
- Resp.
- Exibições
- Últ. msg
-
- 1 Resp.
- 3363 Exibições
-
Últ. msg por VALDECIRTOZZI
-
- 3 Resp.
- 2303 Exibições
-
Últ. msg por VALDECIRTOZZI
-
- 1 Resp.
- 1057 Exibições
-
Últ. msg por VALDECIRTOZZI
-
- 1 Resp.
- 874 Exibições
-
Últ. msg por Tassandro
-
- 1 Resp.
- 2016 Exibições
-
Últ. msg por VALDECIRTOZZI

