10 mL de um hidrocarboneto gasoso são misturados com 100 mL de O2. O sistema sofre combustão seguida de resfriamento, produzindo um volume gasoso igual a 95 mL. A adição de uma solução de KOH provoca a redução do volume gasoso para 75 mL. Os volumes dos gases estão nas MCPT. Determine a fórmula molecular do hidrocarboneto.
R: C2H2
Química Orgânica ⇒ Análise Elementar Tópico resolvido
- VALDECIRTOZZI

- Mensagens: 2569
- Registrado em: 04 Ago 2008, 17:08
- Última visita: 13-10-20
- Agradeceu: 197 vezes
- Agradeceram: 1590 vezes
Fev 2015
26
08:56
Re: Análise Elementar
A equação química que representa a combustão do hidrocarboneto é:
\ O_2 \rightarrow x \ CO_2 + \frac{y}{2}\ H_2O)
Como as condições de medida são as mesmas podemos trabalhar como volumes como se fossem número de mols (Hipótese de Avogadro)
Com o sistema resfriado, o vapor d'água gerado se liquefaz e portanto:

A adição de KOH absorve apenas o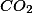 , portanto,
, portanto,  e o volume de gás oxigênio residual é 75 mL. Conclui-se, então, que o volume de gás oxigênio que reagiu com o hidrocarboneto foi 100-75=25 mL.
e o volume de gás oxigênio residual é 75 mL. Conclui-se, então, que o volume de gás oxigênio que reagiu com o hidrocarboneto foi 100-75=25 mL.





Espero ter ajudado!
Como as condições de medida são as mesmas podemos trabalhar como volumes como se fossem número de mols (Hipótese de Avogadro)
Com o sistema resfriado, o vapor d'água gerado se liquefaz e portanto:
A adição de KOH absorve apenas o
Espero ter ajudado!
Editado pela última vez por VALDECIRTOZZI em 26 Fev 2015, 08:56, em um total de 1 vez.
So many problems, so little time!
-
- Tópicos Semelhantes
- Resp.
- Exibições
- Últ. msg
-
- 3 Resp.
- 2275 Exibições
-
Últ. msg por VALDECIRTOZZI
-
- 1 Resp.
- 995 Exibições
-
Últ. msg por VALDECIRTOZZI
-
- 1 Resp.
- 871 Exibições
-
Últ. msg por Tassandro
-
- 1 Resp.
- 1989 Exibições
-
Últ. msg por VALDECIRTOZZI
-
- 0 Resp.
- 1247 Exibições
-
Últ. msg por marguiene

