A pressão exercida por 12 g de um gás ideal na temperatura t, em ºC, num volume v, em litro, é 1,0 atm. Quando a temperatura é aumentada em 10ºC no mesmo volume, a pressão aumentou em 10%. Calcule a temperatura t e o volume v, sabendo que a massa molar do gás é 120 g/mol.
a) -173ºC e 0,82 L
b) -273ºC e 0,82 L
c) 173K e 8,2 L
d) 273K e 8,2 L
e) -373ºC e 8,2 L
Química Geral ⇒ Gases Tópico resolvido
- VALDECIRTOZZI

- Mensagens: 2569
- Registrado em: 04 Ago 2008, 17:08
- Última visita: 13-10-20
- Agradeceu: 197 vezes
- Agradeceram: 1590 vezes
Ago 2014
27
10:32
Re: Gases
Vamos utilizar inicialmente a equação de estado:

Com a transformação é isocórica (isovolumétrica), temos que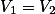 , daí:
, daí:

Lembrando que a temperatura T deve estar em kelvin:

Simplificando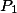 :
:




Com a equação de Clayperon

)

Espero ter ajudado!
Com a transformação é isocórica (isovolumétrica), temos que
Lembrando que a temperatura T deve estar em kelvin:
Simplificando
Com a equação de Clayperon
Espero ter ajudado!
Editado pela última vez por VALDECIRTOZZI em 27 Ago 2014, 10:32, em um total de 1 vez.
So many problems, so little time!
-
- Tópicos Semelhantes
- Resp.
- Exibições
- Últ. msg
-
- 2 Resp.
- 2973 Exibições
-
Últ. msg por oziemilly
-
- 2 Resp.
- 3815 Exibições
-
Últ. msg por mateshowjp
-
- 1 Resp.
- 869 Exibições
-
Últ. msg por VALDECIRTOZZI
-
- 2 Resp.
- 445 Exibições
-
Últ. msg por cicero444
-
- 1 Resp.
- 1125 Exibições
-
Últ. msg por VALDECIRTOZZI

