O Brasil produz, anualmente, cerca de 6.[tex3]10^{6}[/tex3] toneladas de ácido sulfúrico pelo processo de contacto. Em uma das etapas do processo há, em fase gasosa, o equilíbrio
2 SO2 (g) + O2 (g) 2 SO3 (g) KP = 4,0 x [tex3]10^{4}[/tex3]
que se estabelece à pressão total de P atm e temperatura constante. Nessa temperatura, para que o valor da relação [tex3]\frac{x^{2}_{SO_{3}}}{x^{2}_{SO_{2}}x^{1}_{O_{2}}}[/tex3] seja igual a 6,0.[tex3]10^{4}[/tex3], o valor de P deve ser:
x = fração em quantidade de matéria (fração molar) de cada constituinte na mistura gasosa
KP= constante de equilíbrio
Rep:. 1,5
Química Geral ⇒ (FUVEST-SP) Constante de equílibrio
- pklaskoski

- Mensagens: 104
- Registrado em: 28 Jun 2014, 14:19
- Última visita: 24-07-17
- Agradeceu: 65 vezes
- Agradeceram: 5 vezes
Ago 2014
05
19:21
(FUVEST-SP) Constante de equílibrio
Editado pela última vez por pklaskoski em 05 Ago 2014, 19:21, em um total de 1 vez.
- VALDECIRTOZZI

- Mensagens: 2569
- Registrado em: 04 Ago 2008, 17:08
- Última visita: 13-10-20
- Agradeceu: 197 vezes
- Agradeceram: 1590 vezes
Ago 2014
22
10:25
Re: (FUVEST-SP) Constante de Equílibrio
A constanted e equilíbro em termos de pressão parcial é dada por:

lembrando que a pressão parcial é dada por: , em que
, em que  é a fração molar e
é a fração molar e 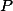 é a pressão total dos sistema. então a expressão do
é a pressão total dos sistema. então a expressão do  fica:
fica:
^2}{{\left(x_{SO_2} \cdot P\right)^2} \cdot {x_{O_2} \cdot P}})



Espero ter ajudado!
lembrando que a pressão parcial é dada por:
Espero ter ajudado!
Editado pela última vez por VALDECIRTOZZI em 22 Ago 2014, 10:25, em um total de 1 vez.
So many problems, so little time!
-
- Tópicos Semelhantes
- Resp.
- Exibições
- Últ. msg
-
- 1 Resp.
- 1284 Exibições
-
Últ. msg por FelipeMartin
-
- 1 Resp.
- 1626 Exibições
-
Últ. msg por MicheleAlves
-
- 1 Resp.
- 2766 Exibições
-
Últ. msg por VALDECIRTOZZI
-
- 1 Resp.
- 2598 Exibições
-
Últ. msg por VALDECIRTOZZI
-
- 6 Resp.
- 8623 Exibições
-
Últ. msg por Vitthor
