Balanceie as equações:
I) [tex3]H_{2}[/tex3][tex3]O_{2}[/tex3]+KMn[tex3]O_{4}[/tex3]+[tex3]H_{2}[/tex3]S[tex3]O_{4}[/tex3][tex3]\rightarrow[/tex3][tex3]K_{2}[/tex3]S[tex3]O_{4}[/tex3]+MnS[tex3]O_{4}[/tex3]+[tex3]H_{2}[/tex3]O+[tex3]O_{2}[/tex3]
II) Mn[tex3]O^{-}_{4}[/tex3]+[tex3]H^{+}[/tex3]+[tex3]H_{2}[/tex3][tex3]O_{2}[/tex3][tex3]\rightarrow[/tex3][tex3]Mn^{2+}[/tex3]+[tex3]H_{2}[/tex3]O+[tex3]O_{2}[/tex3]
Química Geral ⇒ Reações de oxirredução
- pklaskoski

- Mensagens: 104
- Registrado em: 28 Jun 2014, 14:19
- Última visita: 24-07-17
- Agradeceu: 65 vezes
- Agradeceram: 5 vezes
Jul 2014
19
15:46
Reações de oxirredução
Editado pela última vez por pklaskoski em 19 Jul 2014, 15:46, em um total de 1 vez.
-
Auto Excluído (ID:12031)


- Última visita: 31-12-69
Jul 2014
19
18:12
Re: Reações de oxirredução
sempre que a água oxigenada se oxida, agindo como agente redutor, ela gera oxigênio 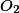 como produto
como produto

[tex3]\Delta Nox = 5[/tex3] Que será o coeficiente do peróxido de hidrogênio

[tex3]\Delta Nox = 2[/tex3] Que será o coeficiente do

balanceando os potássios:

balanceando os manganeses:

balanceando os enxofres:

os hidrogênios:

e os oxigênios:

2-) Mesmo método:

[tex3]\Delta Nox = 5[/tex3] coeficiente do peróxido

[tex3]\Delta Nox = 2[/tex3] coeficiente do manganês
[tex3]2MnO_4^- + H^+ + 5H_2O_2 \rightarrow Mn^{2+} + H_2O + O_2[/tex3]
balanceando o manganês:
[tex3]2MnO_4^- + H^+ + 5H_2O_2 \rightarrow 2Mn^{2+} + H_2O + O_2[/tex3]
O oxigênio da água é oriundo do íon permanganato. Pois o Nox dele é 2. Então balanceamos a água com os oxigênios do permanganato.
[tex3]2MnO_4^- + H^+ + 5H_2O_2 \rightarrow 2Mn^{2+} + 8H_2O + O_2[/tex3]
agora balanceamos os oxigênios restantes:
[tex3]2MnO_4^- + H^+ + 5H_2O_2 \rightarrow 2Mn^{2+} + 8H_2O + 5O_2[/tex3]
por fim os hidrogênios:
[tex3]2MnO_4^- + 6H^+ + 5H_2O_2 \rightarrow 2Mn^{2+} + 8H_2O + 5O_2[/tex3]
[tex3]\Delta Nox = 5[/tex3] Que será o coeficiente do peróxido de hidrogênio
[tex3]\Delta Nox = 2[/tex3] Que será o coeficiente do
balanceando os potássios:
balanceando os manganeses:
balanceando os enxofres:
os hidrogênios:
e os oxigênios:
2-) Mesmo método:
[tex3]\Delta Nox = 5[/tex3] coeficiente do peróxido
[tex3]\Delta Nox = 2[/tex3] coeficiente do manganês
[tex3]2MnO_4^- + H^+ + 5H_2O_2 \rightarrow Mn^{2+} + H_2O + O_2[/tex3]
balanceando o manganês:
[tex3]2MnO_4^- + H^+ + 5H_2O_2 \rightarrow 2Mn^{2+} + H_2O + O_2[/tex3]
O oxigênio da água é oriundo do íon permanganato. Pois o Nox dele é 2. Então balanceamos a água com os oxigênios do permanganato.
[tex3]2MnO_4^- + H^+ + 5H_2O_2 \rightarrow 2Mn^{2+} + 8H_2O + O_2[/tex3]
agora balanceamos os oxigênios restantes:
[tex3]2MnO_4^- + H^+ + 5H_2O_2 \rightarrow 2Mn^{2+} + 8H_2O + 5O_2[/tex3]
por fim os hidrogênios:
[tex3]2MnO_4^- + 6H^+ + 5H_2O_2 \rightarrow 2Mn^{2+} + 8H_2O + 5O_2[/tex3]
Editado pela última vez por Auto Excluído (ID:12031) em 19 Jul 2014, 18:12, em um total de 1 vez.
-
- Tópicos Semelhantes
- Resp.
- Exibições
- Últ. msg
-
- 6 Resp.
- 2181 Exibições
-
Últ. msg por pklaskoski
-
- 1 Resp.
- 3712 Exibições
-
Últ. msg por Brunoranery
-
- 1 Resp.
- 2206 Exibições
-
Últ. msg por MatheusBorges
-
- 1 Resp.
- 1131 Exibições
-
Últ. msg por undefinied3
-
- 1 Resp.
- 1606 Exibições
-
Últ. msg por MatheusBorges
