Oii Luana, tudo bom?
te falar que passei por isso faz pouco tempo kkk; há pouco mais de um ano atrás eu não sabia absolutamente nada de nada (principalmente química), então, não sei qual o caminho que vc passou mas saiba que eventualmente, com esforço e tentativa/erro (haja erros kk), as coisas passam a fazer mais sentido

.
sobre suas dúvidas, vamos lá:
densidade: eu gosto de imaginar a densidade como a concentração de massa no espaço (até porque volume é espaço); então, tratando de quimica, imagina que pra um mesmo volume (por exemplo, um copo de água) você consegue colocar diferentes quantidades de substâncias, a fim de enchê-lo, de acordo com o espaço que elas preenchem - quanto maior a quantidade de uma substância que cabe nesse copo, maior vai ser a massa, e por consequência, maior a densidade.
Mol é algo um pouco mais vago, mas fica mais simples se você comparar ele com outras medidas, a fim de entender um pouco melhor; por exemplo, quando medimos uma rodovia, que costuma ligar cidades muito distantes entre si, ficaria um pouco inviável medir em metros (imagina as placas falandos "são paulo - 8790000 m" kk), dessa forma, nós utilizamos o prefixo kilo, que significa mil - ou seja, 1km é igual a um metro vezes mil. De forma semelhante, quando falamos de quantidade de matéria, a nível atômico/molecular, temos medidas absurdamente pequenas (pra ter uma idéia, em um milimetro cabem 10 milhões de átomos e cada átomo, no caso do hidrogênio, pesa 0,000000000...mais alguns zeros ... 001 grama kk); pra facilitar isso, estabeleceu-se um sistema de multiplos de átomo: não sei se você conhece a unidade de massa atômica (u), mas ela é definida como 1/12 partes da massa de um átomo de carbono, o que equivale a massa de um próton ou neutron; essa medida(u), aliás, vale 1,6 x 10^-24 gramas - uma massa muito pequena. Agora, imagina se você tivesse que trabalhar com o numero de átomos pra medidas como 3, 4 , 16 gramas ( a matemática por trás disso ficaria um pouco chato de ficar abordando sempre que precisasse) - e é aí, que entra nosso amigo MOL - como quase sempre as medidas trabalhadas são em gramas, o que foi feito é basicamente achar o numero de unidades de massa atômica (u) - a tal massa de um próton/neutron - necessária para chegar em uma grama, o que pode ser feito por regra de 3:
1u --->1,6x10^-24grama
xu ---> 1 grama
o resultado, que é o saudoso mol, vou deixar pra você calcular

o.b.s: uma consequência legal é que, como a tabela periódica é medida em unidade de massas atômicas (já que indica a massa - que nada mais é que a soma de prótons e neutrons), um mol de qualquer elemento vai ser igual a massa indicada na tabela em gramas, por exemplo : um mol de cloro (massa = 35 u, 17 prótons + 18 neutrons) = 35 gramas de cloro.
agora, pra finalizar, geometria foi algo que eu me enfezei bastante também kkk (essa foi umas das coisas que eu mais errei até realmente entender); de forma simplificada, nós sabemos que os elétrons se repelem, certo? Mas, como que um átomo se mantêm estável após uma reação então? através da mudança da sua configuração eletrônica!
Pelo modelo do átomo de bohr, temos o nucleo com regiões onde os elétrons possuem maior probabilidade de estar. Utilizando da distribuição de summerfield (aquele famoso 1s2, 2s2, 2p6, 3s2 ...), nós estamos, na verdade, distribuindo os elétrons em configurações estáveis entre si. Quando, por algum motivo maior (como um átomo mais eletronegativo), seus elétrons precisam mudar de posição, acontece o que chamamos de transição eletrônica; nesse momento, pode haver a formação de orbitais hibridos, como segue na imagem:

- transferir.jpg (8.47 KiB) Exibido 1467 vezes
A questão dos orbitais acho que ficaria muito dificil de explicar; então segue um link com algumas explicações muito boas:
https://www.youtube.com/watch?v=YEHsnV6fxGAhttps://www.youtube.com/watch?v=zNEg8XBFOAc&t=232sAgoraaa, um macete (que acho muito estranho o fato de não ser comentado):
(I)quase sempre, a soma das letras do orbital hibrido indicam o numero de ligantes, por exemplo:
sp : s=1/p=2 --- s+p = 2 ligantes
sp2: s=1/p2=1x2 --->s+2xp = 3 ligantes
sp3: s=1/p3=1x3 --->s+2xP = 4 ligantes
...
(II)agora que nós sabemos o numero de ligantes, é só arranjar eles numa conformação espacial na qual eles fiquem mais distantes entre si possível, por exemplo:
sp= 2 ligantes ---> maior distância = 180 graus = geometria linear
sp2= 3 ligantes ---> maior distância = 120 graus = geometria trigonal plana
sp3 = 4 ligantes ---> maior distância = 109 grau (agora vai ficar 3D) = geometria tetraédrica
...
compara essa idéia com a seguinte tabela:
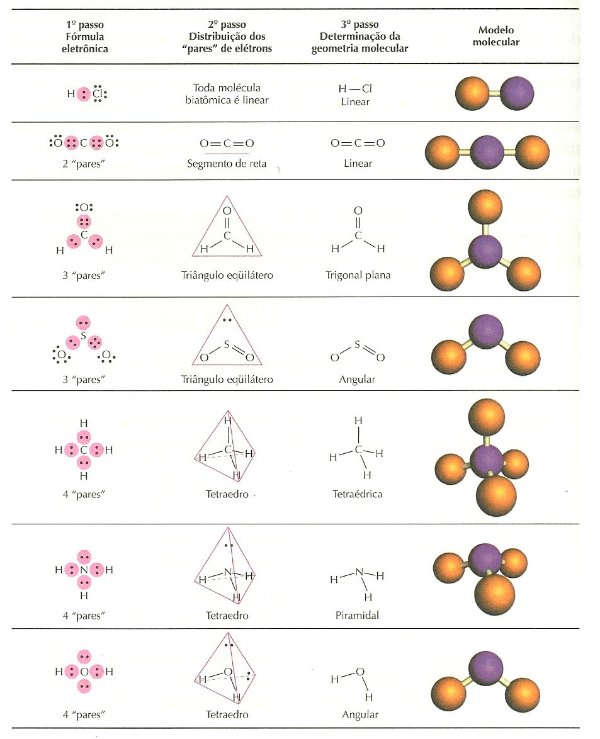
- geometria-molecular-passo-a-passo.jpg (62.09 KiB) Exibido 1467 vezes
basicamente, são essas a idéias; quanto à dificuldade de entrar as coisas na cachola algumas vezes, relaxa que faz parte - quando vc menos esperar, as coisas que pareciam impossíveis antes vão se tornar triviais.
desculpa pelo textão e espero ter ajudado

