Demonstração - modelo atômico de Bohr
Enviado: Sex 27 Jul, 2012 02:10
------------------------------------------------------------------------------
Hipótese:
Considere um átomo de hidrogênio representado abaixo. Sendo ,
, 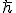 ,
, 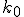 e
e 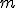 a carga elétrica elementar, o momento angular do elétron, a constante eletrostática do vácuo e a massa do elétron.
Mostre que o raio de Bohr (
a carga elétrica elementar, o momento angular do elétron, a constante eletrostática do vácuo e a massa do elétron.
Mostre que o raio de Bohr (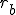 ) e a energia mecânica (
) e a energia mecânica (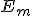 ) do elétron são dados por:
) do elétron são dados por:
 e
e ) onde
onde 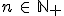 .
.
-------------------------------------------------------------------------------
Demonstração:
A força de atração eletrostática é a resultante centrípeta. Nesse caso, podemos fazer)
Da definição de momento angular de uma partícula elementar em um raio de Bohr, tiramos:
)
Substituindo) em
em ) , encontramos:
, encontramos:
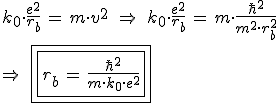
A energia mecânica total do elétron em uma orbital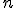 qualquer é dada por:
qualquer é dada por:
%7D%7Br_%7Bn%7D%7D%20%5C,%5C,%5C,%5C,%5C,%5C,%5C,%20(III))
De) e
e ) , tiramos:
, tiramos:
)
Conforme os postulados de Bohr, temos:
%5C,%5C,%5C,%5C,%5C,%5C,%5C,%20(V))
De) e
e ) , tiramos:
, tiramos:
)
Substituindo o valor de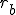 encontrado na expressão acima, vem:
encontrado na expressão acima, vem:
%5Cleft(%5Cfrac%7B1%7D%7Bn%5E%7B2%7D%7D%5Cright)%20%5C,%5C,%5C,%20%5CRightarrow%20%5C,%5C,%5C,%20%5Cboxed%7B%5Cboxed%7B%20E_%7Bm%7D%20%5C,%20=%20%5C,%20-%20%5C,%20%5Cfrac%7Bm%20%5Ccdot%20k_%7B0%7D%5E%7B2%7D%20%5Ccdot%20e%5E%7B4%7D%7D%7B2%20%5Ccdot%20%5Chbar%5E%7B2%7D%7D%20%5Ccdot%20%5Cleft(%5Cfrac%7B1%7D%7Bn%7D%5Cright)%7D%7D)
Essa foi uma forma que eu criei de demonstrar os postulados de Bohr sem utilizar mecânica estatística.
Espero que gostem!
Hipótese:
Considere um átomo de hidrogênio representado abaixo. Sendo
-------------------------------------------------------------------------------
Demonstração:
A força de atração eletrostática é a resultante centrípeta. Nesse caso, podemos fazer
Da definição de momento angular de uma partícula elementar em um raio de Bohr, tiramos:
Substituindo
A energia mecânica total do elétron em uma orbital
De
Conforme os postulados de Bohr, temos:
De
Substituindo o valor de
Essa foi uma forma que eu criei de demonstrar os postulados de Bohr sem utilizar mecânica estatística.
Espero que gostem!