IME/ITA ⇒ (IME) Efusão de gases Tópico resolvido
Moderador: [ Moderadores TTB ]
-
BushJunior

- Mensagens: 141
- Registrado em: Dom 16 Dez, 2012 18:05
- Última visita: 14-02-16
Jul 2013
03
13:13
(IME) Efusão de gases
Um cilindro contendo oxigênio puro teve sua pressão reduzida de 2,6atm para 2 atm, em 47 min, devido a um vazamento através de um pequeno orifício existente. Quando cheio com outro gás, n mesma pressão inicial, levou 55,1 min para que a pressão caísse outra vez ao valor de 2 atm.Determine a massa molecular do segundo gás.Considere que ambos os processos foram isotérmicos e à mesma temperatura, e que os gases nestas condições de pressão e temperatura apresentam comportamento ideal.
“Bem, todos morrem um dia, é simples matemática. Nada de novo. A espera é que é um problema”. (Charles Bukowski)
Jul 2013
04
15:52
Re: (IME) Efusão de gases
Para o oxigênio a velocidade é:

Similarmente, para o outro gás a velocidade é
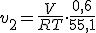
------
Substituindo na equação
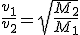

Vamos achar
Similarmente, para o outro gás a velocidade é
------
Substituindo na equação
Vamos achar
Última edição: Radius (Qui 04 Jul, 2013 15:52). Total de 1 vez.
-
BushJunior

- Mensagens: 141
- Registrado em: Dom 16 Dez, 2012 18:05
- Última visita: 14-02-16
Jul 2013
05
09:01
Re: (IME) Efusão de gases
Não compreendi muito bem a equação v1, vc poderia me explicar como chegar nela ?
“Bem, todos morrem um dia, é simples matemática. Nada de novo. A espera é que é um problema”. (Charles Bukowski)
Jul 2013
05
09:34
Re: (IME) Efusão de gases
bom, a velocidade pode ser em metros por segundo, metros cúbicos por segundo, atmosferas por segundo, qualquer coisa.
No caso eu preferi usar mols/segundo. Usando Clapeyron, com V, R e T constantes:
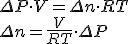
então a velocidade do oxigênio é . Entendido?
. Entendido?
No caso eu preferi usar mols/segundo. Usando Clapeyron, com V, R e T constantes:
então a velocidade do oxigênio é
Última edição: Radius (Sex 05 Jul, 2013 09:34). Total de 1 vez.
-
BushJunior

- Mensagens: 141
- Registrado em: Dom 16 Dez, 2012 18:05
- Última visita: 14-02-16
Jul 2013
05
14:30
Re: (IME) Efusão de gases
Acredito que dê para fazer pelas leis de Graham de efusão.
[tex3]\frac{V1}{V2}[/tex3] = ([tex3]\sqrt{\frac{M2}{M1}}[/tex3] )
[tex3]\frac{V1}{V2} = \frac{t2}{t1}[/tex3] (como são grandezas inversamente proporcionais)
[tex3]\frac{t2}{t1} = \sqrt{\frac{M2}{M1}}[/tex3]
Substituí aqui e deu 43,980 g/mol.
[tex3]\frac{V1}{V2}[/tex3] = ([tex3]\sqrt{\frac{M2}{M1}}[/tex3] )
[tex3]\frac{V1}{V2} = \frac{t2}{t1}[/tex3] (como são grandezas inversamente proporcionais)
[tex3]\frac{t2}{t1} = \sqrt{\frac{M2}{M1}}[/tex3]
Substituí aqui e deu 43,980 g/mol.
Última edição: BushJunior (Sex 05 Jul, 2013 14:30). Total de 1 vez.
“Bem, todos morrem um dia, é simples matemática. Nada de novo. A espera é que é um problema”. (Charles Bukowski)
-
BushJunior

- Mensagens: 141
- Registrado em: Dom 16 Dez, 2012 18:05
- Última visita: 14-02-16
Jul 2013
05
14:32
Re: (IME) Efusão de gases
Entendi sim, obrigado.
“Bem, todos morrem um dia, é simples matemática. Nada de novo. A espera é que é um problema”. (Charles Bukowski)
-
- Tópicos Semelhantes
- Respostas
- Exibições
- Última msg
-
- 0 Respostas
- 1033 Exibições
-
Última msg por careca
-
- 2 Respostas
- 1213 Exibições
-
Última msg por iammaribrg
-
- 1 Respostas
- 162 Exibições
-
Última msg por παθμ
-
- 0 Respostas
- 724 Exibições
-
Última msg por cloudff7
-
- 2 Respostas
- 1043 Exibições
-
Última msg por maria923








