(ITA) Seja S a solubilidade de Ag3PO4 em 100 g de água pura numa dada temperatura. A seguir, para a mesma temperatura, são feitas as seguintes afirmações a respeito da solubilidade de Ag3P04 em 100 g de diferentes soluções aquosas:
I. A solubilidade do Ag3PO4 em solução aquosa 1 mol/L de HNO3 é maior do que S.
II. A solubilidade do Ag3PO4 em solução aquosa 1 mol/L de AgNO3 é menor do que S.
III. A solubilidade do Ag3PO4 em solução aquosa 1 mol/L de Na3PO4 é menor do que S.
IV. A solubilidade do Ag3PO4 em solução aquosa 1 mol/L de KCN é maior do que S.
V. A solubilidade do Ag3PO4 em solução aquosa 1 mol/L de NaNO3 é praticamente igual a S.
Dessas afirmações, estão CORRETAS:
a) apenas I, II e III.
b) apenas I, III e IV.
c) apenas II, III e IV.
d) apenas II, III e V.
e) todas.
IME/ITA ⇒ (ITA) Solubilidade
Moderador: [ Moderadores TTB ]
-
VALDECIRTOZZI

- Mensagens: 2569
- Registrado em: Seg 04 Ago, 2008 17:08
- Última visita: 13-10-20
Dez 2012
19
14:51
Re: (ITA) Solubilidade
Consideremos o equilíbrio:
%7D%20%5Cleftrightharpoons3Ag%5E+_%7B(aq)%7D+PO_4_%7B(aq)%7D%5E%7B3-%7D)
I) Está correta, pois a ao adicionarmos o em uma solução de ácido nítrico há a formação de
em uma solução de ácido nítrico há a formação de 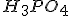 , que é um ácido fraco, deslocando o equilíbrio para a direita, dissolvendo mais
, que é um ácido fraco, deslocando o equilíbrio para a direita, dissolvendo mais  .
.
II) Está correta. Em meio rico de íons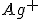 , pelo efeito do íon comum o equilibrio se desloca para a esquerda,diminuindo a solubilidade do sal.
, pelo efeito do íon comum o equilibrio se desloca para a esquerda,diminuindo a solubilidade do sal.
III) Está correta, pelos mesmos motivos de (II).
IV) Está correta pois em meio rico de ions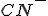 , há formação do complexo
, há formação do complexo _2%5E-) , conforme a reação:
, conforme a reação: %7D+%206CN_%7B(aq)%7D%5E-%20%5Cleftrightharpoons%203Ag(CN)_%7B2(aq)%7D%5E-+PO_4_%7B(aq)%7D%5E%7B3-%7D) , o íon prata é consumido e o equilíbrio se desloca para a direita.
, o íon prata é consumido e o equilíbrio se desloca para a direita.
V) Está correta. Pois com nitrato de sódio, não há formação de complexos, ácidos fracos ou deslocamento de equilíbrio.
Alternativa
Espero ter ajudado!
I) Está correta, pois a ao adicionarmos o
II) Está correta. Em meio rico de íons
III) Está correta, pelos mesmos motivos de (II).
IV) Está correta pois em meio rico de ions
V) Está correta. Pois com nitrato de sódio, não há formação de complexos, ácidos fracos ou deslocamento de equilíbrio.
Alternativa
Espero ter ajudado!
Última edição: VALDECIRTOZZI (Qua 19 Dez, 2012 14:51). Total de 1 vez.
So many problems, so little time!
Dez 2012
19
22:43
Re: (ITA) Solubilidade
Valdecirtozzi,
Tentei provar a alternativa II por meio de cálculos químicos, observe:
%7D%20%5Cleftrightharpoons3Ag%5E+_%7B(aq)%7D+PO_4_%7B(aq)%7D%5E%7B3-%7D)
![Kps = [Ag^{+}]^3 \cdot[PO_4^{3-}] Kps = [Ag^{+}]^3 \cdot[PO_4^{3-}]](https://www.tutorbrasil.com.br/latex/mimetex_.cgi?Kps%20=%20%5BAg%5E%7B+%7D%5D%5E3%20%5Ccdot%5BPO_4%5E%7B3-%7D%5D)
![[Ag^+]^3 = 3M [Ag^+]^3 = 3M](https://www.tutorbrasil.com.br/latex/mimetex_.cgi?%5BAg%5E+%5D%5E3%20=%203M)
![[PO_4^{3-}] = M [PO_4^{3-}] = M](https://www.tutorbrasil.com.br/latex/mimetex_.cgi?%5BPO_4%5E%7B3-%7D%5D%20=%20M)
Sendo S a solubilidade do fosfato de prata, temos que:
![S= [3M]^3\cdot [M] S= [3M]^3\cdot [M]](https://www.tutorbrasil.com.br/latex/mimetex_.cgi?S=%20%5B3M%5D%5E3%5Ccdot%20%5BM%5D)

Adicionando Nitrato de Prata
%7D%20%5Cleftrightharpoons%20Ag%5E+_%7B(aq)%7D+NO_3_%7B(aq)%7D%5E%7B-%7D)
![[Ag^+] = 1mol/L [Ag^+] = 1mol/L](https://www.tutorbrasil.com.br/latex/mimetex_.cgi?%5BAg%5E+%5D%20=%201mol/L)
![[NO_3^-] = 1mol/L [NO_3^-] = 1mol/L](https://www.tutorbrasil.com.br/latex/mimetex_.cgi?%5BNO_3%5E-%5D%20=%201mol/L)
Pelo efeito do íon comum teremos um novo valor para o Kps do fosfato de prata, desse modo:
![[Ag^+]^3 = 3M + 1 \approx 1 [Ag^+]^3 = 3M + 1 \approx 1](https://www.tutorbrasil.com.br/latex/mimetex_.cgi?%5BAg%5E+%5D%5E3%20=%203M%20+%201%20%5Capprox%201) (Posso fazer esta aproximação?)
(Posso fazer esta aproximação?)
![[PO_4^{3-}] = M [PO_4^{3-}] = M](https://www.tutorbrasil.com.br/latex/mimetex_.cgi?%5BPO_4%5E%7B3-%7D%5D%20=%20M)
![Kps = [Ag^{+}]^3 \cdot[PO_4^{3-}] Kps = [Ag^{+}]^3 \cdot[PO_4^{3-}]](https://www.tutorbrasil.com.br/latex/mimetex_.cgi?Kps%20=%20%5BAg%5E%7B+%7D%5D%5E3%20%5Ccdot%5BPO_4%5E%7B3-%7D%5D)
![S'= [1]^3\cdot [M] S'= [1]^3\cdot [M]](https://www.tutorbrasil.com.br/latex/mimetex_.cgi?S'=%20%5B1%5D%5E3%5Ccdot%20%5BM%5D)
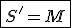
Desse modo concluímos que a solubilidade diminui, pois fica comprovado que

Há alguma incoerência ou erro? Você concorda com o raciocínio?
Obrigado.
Tentei provar a alternativa II por meio de cálculos químicos, observe:
Sendo S a solubilidade do fosfato de prata, temos que:
Adicionando Nitrato de Prata
Pelo efeito do íon comum teremos um novo valor para o Kps do fosfato de prata, desse modo:
Desse modo concluímos que a solubilidade diminui, pois fica comprovado que
Há alguma incoerência ou erro? Você concorda com o raciocínio?
Obrigado.
Última edição: Diegooo (Qua 19 Dez, 2012 22:43). Total de 1 vez.
-
VALDECIRTOZZI

- Mensagens: 2569
- Registrado em: Seg 04 Ago, 2008 17:08
- Última visita: 13-10-20
Dez 2012
20
07:50
Re: (ITA) Solubilidade
Bom dia, Diego! A princípio seu modo de pensar está correto! Eu faria algo bem parecido!
Um abraço!
Um abraço!
So many problems, so little time!
Out 2016
26
12:41
Re: (ITA) Solubilidade
VALDECIRTOZZI, como eu sei se formará um complexo? Não entendi.
-
- Tópicos Semelhantes
- Respostas
- Exibições
- Última msg









