Página 1 de 1
(ITA - 1999) Soluções
Enviado: Qua 12 Dez, 2012 22:46
por mahriana
Para preparar 80 l de uma solução aquosa 12 % (massa/massa) de KOH (massa específica da solução = 1,0 g/cm3) foram adicionados x litros de uma solução aquosa 44 % (massa/massa) de KOH (massa específica da solução = 1,5 g/cm3) e y litros de água deionizada (massa específica = 1,0 g/cm3).Os valores de x e y são respectivamente:
A. 12 L e 68 L.
B. 16 L e 64 L.
C. 30 L e 50 L.
D. 36 L e 44 L.
E. 44 L e 36 L.
Re: (ITA - 1999) Soluções
Enviado: Qui 13 Dez, 2012 09:55
por VALDECIRTOZZI
Veja bem, eu achei estranho a solução 12% de KOH ter a mesma densidade da água deionizada, conforme seu enunciado. Os resultados não batiam com nenhuma das alternativas. Após alguns cálculos, creio que a densidade da solução de KOH 12% deva ser 1,1 g/cm³. Se for isso temos:
A solução 44% em massa terá a seguinte concentração em g/L:
Há 44 g de KOH em 100 g de solução.
100 g de solução, utilizando a densidade de 1,5 g/cm³ será:
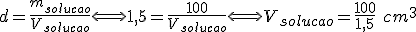
=%5Cfrac%7Bm_%7Bsoluto%7D%7D%7BV_%7Bsolucao%7D%7D%20%5CLongleftrightarrow%20C%20%5Cleft(g/%20%5Cell%5Cright)%20=%20%5Cfrac%7B44%7D%7B%5Cfrac%7B100%7D%7B1,5%7D%20%5C%20.%20%5C%2010%5E%7B-3%7D%7D=660%20%5C%20g/%20%5Cell)
Cálculo da concentração final da solução de KOH: de forma análoga:
Há 12 g de KOH em 100 g de solução.
100 g de solução, utilizando a densidade de 1,1 g/cm³ será:
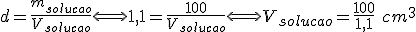
=%5Cfrac%7Bm_%7Bsoluto%7D%7D%7BV_%7Bsolucao%7D%7D%20%5CLongleftrightarrow%20C%20%5Cleft(g/%20%5Cell%5Cright)%20=%20%5Cfrac%7B12%7D%7B%5Cfrac%7B100%7D%7B1,1%7D%20%5C%20.%20%5C%2010%5E%7B-3%7D%7D=132%20%5C%20g/%20%5Cell)
Pela fórmula de diluição temos que:
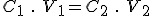
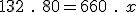
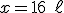
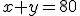
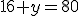
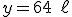
Alternativa
Espero ter ajudado!
Re: (ITA - 1999) Soluções
Enviado: Qui 13 Dez, 2012 10:09
por mahriana
Muito Obrigado já havia tentado várias vezes com esses dados realmente o enunciado diz "KOH(massa específica da solução = 1,10 g/cm3 )"