( ITA - 2001 ) Equilíbrio Químico
Enviado: Ter 26 Jun, 2012 17:10
Eu sei classificar as alternativas como corretas, tendo problema apenas quanto à alternativa D, que é a resposta. Gostaria que alguém explicasse por que a D é errada, se a concentração de um sólido é constante.
Sulfato de cobre penta - hidratado (%7D) ) é colocado em um recipiente fechado, de volume constante, previamente evacuado, provido de um medidor de pressão e de um dispositivo de entrada/saída para reagentes. A 25º C é estabelecido, dentro do recipiente, o equilíbrio representado pela equação química:
) é colocado em um recipiente fechado, de volume constante, previamente evacuado, provido de um medidor de pressão e de um dispositivo de entrada/saída para reagentes. A 25º C é estabelecido, dentro do recipiente, o equilíbrio representado pela equação química: %7D%20%5C,%5C,%5C,%20%5Crightleftharpoons%20%5C,%5C,%5C,%20CuSO_%7B4%7D%20%5Ccdot%203H_%7B2%7DO_%7B(c)%7D%20%5C,%20+%20%5C,%202%20%5C,%20H_%7B2%7DO_%7B(g)%7D)
Quando o equilíbrio é atingido, a pressão dentro do recipiente é igual a 7,6 mmHg. A seguir, a pressão de vapor da água é aumentada para 12 mmHg e um novo equilíbrio é restabelecido na mesma temperatura. A respeito do efeito de aumento da pressão de vapor de água sobre o equilíbrio de dissociação do%7D) , qual das opções seguintes contém a afirmação ERRADA?
, qual das opções seguintes contém a afirmação ERRADA?
a) o valor da constante de equilíbrio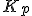 é igual a
é igual a 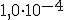 .
.
b) a quantidade de água na fase gasosa permanece praticamente inalterada.
c) A concentração (mol/L) de água na fase%7D) permanece inalterada.
permanece inalterada.
d) A concentração em (mol/L) de água na fase sólida total permanece inalterada.
e) A massa total do conteúdo do recipiente aumenta.
Sulfato de cobre penta - hidratado (
Quando o equilíbrio é atingido, a pressão dentro do recipiente é igual a 7,6 mmHg. A seguir, a pressão de vapor da água é aumentada para 12 mmHg e um novo equilíbrio é restabelecido na mesma temperatura. A respeito do efeito de aumento da pressão de vapor de água sobre o equilíbrio de dissociação do
a) o valor da constante de equilíbrio
b) a quantidade de água na fase gasosa permanece praticamente inalterada.
c) A concentração (mol/L) de água na fase
d) A concentração em (mol/L) de água na fase sólida total permanece inalterada.
e) A massa total do conteúdo do recipiente aumenta.