Olá!
Você precisa fazer o balanceamento da equação química, e a única forma de achar a resposta correta é utilizando o método do íon elétron. Se você não conhece esse método procure a respeito, pois ele é muito importante. Tentarei explicar ao máximo no decorrer da resolução do problema.
Primeiramente ache quem está oxidando e quem está reduzindo.
No caso temos:
%7D~%5Crightarrow%20~Mn%5E%7B2+%7D_%7B(aq)%7D)
%7D~%5Crightarrow%20~CO_%7B2(g)%7D)
Essas são as reações que iremos fazer. Primeiro trabalharemos na Redução.
A primeira coisa a se fazer é balancear os átomos que estão presentes na reação, perceba que há um manganês nos produtos e um manganês nos reagentes, porém há 4 átomos de oxigênio nos produtos e nenhum nos reagentes, então adicionaremos 4 moléculas de água nos produtos.
%7D~%5Crightarrow%20~Mn%5E%7B2+%7D_%7B(aq)%7D~~+~~4H_%7B2%7DO_%7B(l)%7D)
Agora iremos balancear os átomos de hidrogênio, adicionando 8 íons
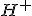
%7D~~+~~8H%5E%7B+%7D_%7B(aq)%7D~%5Crightarrow%20~Mn%5E%7B2+%7D_%7B(aq)%7D~~+~~4H_%7B2%7DO_%7B(l)%7D)
Agora precisamos balancear as cargas.
%7D~~+~~8H%5E%7B+%7D_%7B(aq)%7D~~+~~5e%5E%7B-%7D~%5Crightarrow%20~Mn%5E%7B2+%7D_%7B(aq)%7D~~+~~4H_%7B2%7DO_%7B(l)%7D)
A semi-reação de Redução está balanceada. Agora vamos para a Oxidação.
Seguindo o mesmo passo e balanceando os átomos que já se encontram na semi-reação:
%7D~%5Crightarrow%20~2CO_%7B2(g)%7D)
Balanceando as cargas:
%7D~%5Crightarrow%20~2CO_%7B2(g)%7D~~+~~2e%5E%7B-%7D)
Então temos:
%7D~~+~~8H%5E%7B+%7D_%7B(aq)%7D~~+~~5e%5E%7B-%7D~%5Crightarrow%20~Mn%5E%7B2+%7D_%7B(aq)%7D~~+~~4H_%7B2%7DO_%7B(l)%7D)
%7D~%5Crightarrow%20~2CO_%7B2(g)%7D~~+~~2e%5E%7B-%7D)
A equação global é a soma dessas semi-reações, porém perceba que as cargas devem se cancelar, com isso, basta multiplicar a semi-reação de oxidação por 5 e a semi-reação de redução por 2.
%7D~~+~~16H%5E%7B+%7D_%7B(aq)%7D~~+~~10e%5E%7B-%7D~%5Crightarrow%20~2Mn%5E%7B2+%7D_%7B(aq)%7D~~+~~8H_%7B2%7DO_%7B(l)%7D)
%7D~%5Crightarrow%20~10CO_%7B2(g)%7D~~+~~10e%5E%7B-%7D)
Basta olhar para a semi-reação de redução que você perceberá a resposta correta. Caso queira a reação global basta somar as duas semi-reações.









