Considere os sistemas químicos descritos a seguir.
I. Uma mistura de hidrogênio, iodo e iodeto de hidrogênio é introduzida num recipiente aquecido a 783 K. Cada um dos componentes da mistura se encontra no estado gasoso e na concentração de 2,00 .10^(-3) mol/L. Nesse sistema ocorre a reação:
[tex2]H_2_{ (g) }+ I_2_{ (g)}\rightleftharpoons 2 HI _{(g)}[/tex2]
cuja constante de equilíbrio é igual a 46.
II. Uma mistura de [tex2]N_2_{ (g)}[/tex2], [tex2]O_2_{ (g)}[/tex2] e [tex2]NO_{ (g)}[/tex2] é introduzida num recipiente aquecido a 800 K. A concentração de cada um dos seus componentes é igual a [tex2]2,00. 10^{-3} \ mol/L[/tex2]. Nesse sistema ocorre a reação:
[tex2]N_2_{ (g) }+ O_2_{ (g)} \rightleftharpoons 2 NO_{ (g)}[/tex2]
cuja constante de equilíbrio é igual a [tex2]3,40 \cdot 10^{-21}.[/tex2]
Sobre os sistemas I e II, o que é correto afirmar?
a) As constantes de equilíbrio indicam que a velocidade da reação no sistema I é maior que a velocidade da reação no sistema II.
b) Quando o sistema I atinge o estado de equilíbrio, predomina a espécie HI.
c) Quando o sistema II atinge o estado de equilíbrio, predomina a espécie NO.
d) No sistema I, ocorre o consumo de gás hidrogênio até que o estado de equilíbrio seja atingido.
e) No sistema II, a concentração do gás nitrogênio aumenta até que o estado de equilíbrio seja atingido.
f) No sistema II, após o equilíbrio ser atingido, a concentração de oxigênio é igual à concentração de nitrogênio.
a resposta é: b, d, e, f
ALGUÉM PODE ME EXPLICAR O PORQUÊ DE CADA UMA?
POR FAVOR
Química Geral ⇒ (UFPR) Equilíbrio Químico
Moderador: [ Moderadores TTB ]
Ago 2016
18
23:51
(UFPR) Equilíbrio Químico
Última edição: gamimaru (Qui 18 Ago, 2016 23:51). Total de 3 vezes.
-
VALDECIRTOZZI

- Mensagens: 2569
- Registrado em: Seg 04 Ago, 2008 17:08
- Última visita: 13-10-20
Ago 2016
26
07:36
Re: (UFPR) Equilíbrio Químico
No primeiro equilíbrio, a expressão da constante de equilíbrio é dada por:
![46=\frac{\left[HI_{(g)}\right]^2}{\left[HI_{(g)}\right] \cdot \left[I_2_{(g)}\right]} 46=\frac{\left[HI_{(g)}\right]^2}{\left[HI_{(g)}\right] \cdot \left[I_2_{(g)}\right]}](https://www.tutorbrasil.com.br/latex/mimetex_.cgi?46=%5Cfrac%7B%5Cleft%5BHI_%7B(g)%7D%5Cright%5D%5E2%7D%7B%5Cleft%5BHI_%7B(g)%7D%5Cright%5D%20%5Ccdot%20%5Cleft%5BI_2_%7B(g)%7D%5Cright%5D%7D)
Já no segundo equilíbrio temos a seguinte expressão:
![3,40 \cdot 10^{-21}=\frac{\left[NO_{(g)}\right]^2}{\left[N_2_{(g)}\right] \cdot \left[O_2_{(g)}\right]} 3,40 \cdot 10^{-21}=\frac{\left[NO_{(g)}\right]^2}{\left[N_2_{(g)}\right] \cdot \left[O_2_{(g)}\right]}](https://www.tutorbrasil.com.br/latex/mimetex_.cgi?3,40%20%5Ccdot%2010%5E%7B-21%7D=%5Cfrac%7B%5Cleft%5BNO_%7B(g)%7D%5Cright%5D%5E2%7D%7B%5Cleft%5BN_2_%7B(g)%7D%5Cright%5D%20%5Ccdot%20%5Cleft%5BO_2_%7B(g)%7D%5Cright%5D%7D)
Item a) é falso, pois as constantes de equilíbrio não nos dizem nada sobre a cinética das reações, apenas indicam as razões entre as quantidades das espécies no equilíbrio.
Item b) é verdadeiro como há predomínio dos produtos na reação quando se atinge o equilíbrio.
há predomínio dos produtos na reação quando se atinge o equilíbrio.
Item c) é falso, como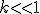 há predomínio dos reagentes na reação quando se atinge o equilíbrio.
há predomínio dos reagentes na reação quando se atinge o equilíbrio.
Item d) é verdadeiro, há consumo dos reagentes para se formar o HI, pois está é a espécie que estará predominante no equilíbrio.
Item e) é verdadeiro, como a constante de equilíbrio é muito pequena, há predomínio dos reagentes no quando o equilíbrio for atingido.
item f) é verdadeiro, como as constantes estequiométricas são iguais para ambos os gases e as concentrações iniciais também eram iguais, quando o equilíbrio for atingido suas quantidades serão iguais.
serão iguais.
Espero ter ajudado!
Já no segundo equilíbrio temos a seguinte expressão:
Item a) é falso, pois as constantes de equilíbrio não nos dizem nada sobre a cinética das reações, apenas indicam as razões entre as quantidades das espécies no equilíbrio.
Item b) é verdadeiro como
Item c) é falso, como
Item d) é verdadeiro, há consumo dos reagentes para se formar o HI, pois está é a espécie que estará predominante no equilíbrio.
Item e) é verdadeiro, como a constante de equilíbrio é muito pequena, há predomínio dos reagentes no quando o equilíbrio for atingido.
item f) é verdadeiro, como as constantes estequiométricas são iguais para ambos os gases e as concentrações iniciais também eram iguais, quando o equilíbrio for atingido suas quantidades
Espero ter ajudado!
Última edição: VALDECIRTOZZI (Sex 26 Ago, 2016 07:36). Total de 2 vezes.
So many problems, so little time!
-
- Tópicos Semelhantes
- Respostas
- Exibições
- Última msg








