Página 1 de 1
Estequiometria
Enviado: Qua 17 Ago, 2016 21:44
por brunoafa
Muitas minas abandonadas já expuseram comunidades próximas ao problema de drenagem do ácido das minas. Certos mineirais, como a pirita
)
, se decompõem quando expostos ao ar e formam soluções de ácido sulfúrico. A água ácida das minas, passa, então, para lagos e riachos, matando peixes e outros animais. Em uma mina no Colorado, Estados Unidos, uma amostra de
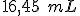
de água de mina foi neutralizada completamente com
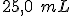
de uma solução
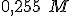
em
)
. Qual é a concentração molar de
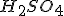
na água?
O ruim para mim é saber como montar a equação. Fico pensando em qual será o produto da reação, tem uma regra prática?
Re: Estequiometria
Enviado: Qui 18 Ago, 2016 06:46
por VALDECIRTOZZI
Trata-se de uma reação de neutralização acido base cuja equação química do processo pode ser assim representada:
É preciso lembrar que ácido mais base dá sal mais água.
%7D+2%5C%20KOH_%7B(aq)%7D%5Clongrightarrow%20K_2SO_4_%7B(aq)%7D+2%5C%20H_2O_%7B(%5Cell)%7D)
O número de mols da base
)
:
%7D=0,25%20%5Ccdot%200,025=0,00625%20%5C%20mol)
Como a estequiometria da reação é 1 mol de ácido para 2 mols de base, temos:
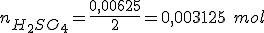
Portanto:
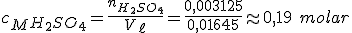
Espero ter ajudado!
Re: Estequiometria
Enviado: Qui 18 Ago, 2016 23:41
por brunoafa
Quando você escreve
%7D)
significa que é
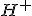
E
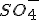
? Porque se for assim fica mais fácil de prever o produto.
No caso como você disse, sal mais base dá sal mais água mas e se fosse uma reação que não tem regra prática?
Re: Estequiometria
Enviado: Sex 19 Ago, 2016 08:04
por VALDECIRTOZZI
Há reações que se consegue prever o produto: se for dupla troca, combustão de composto orgânico, algumas reações de óxido-redução entre outra; contudo é preciso lembrar que uma equação química apenas representa um dado fenômeno químico, ou seja, ela descreve a natureza de forma aproximada; portanto, não há como saber, a prori, quais serão os produtos sem estudá-las previamente.
Claro que há várias que são tão "batidas" que se acaba decorando, ou ficando óbvio o que será formado.
) , se decompõem quando expostos ao ar e formam soluções de ácido sulfúrico. A água ácida das minas, passa, então, para lagos e riachos, matando peixes e outros animais. Em uma mina no Colorado, Estados Unidos, uma amostra de
, se decompõem quando expostos ao ar e formam soluções de ácido sulfúrico. A água ácida das minas, passa, então, para lagos e riachos, matando peixes e outros animais. Em uma mina no Colorado, Estados Unidos, uma amostra de 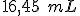 de água de mina foi neutralizada completamente com
de água de mina foi neutralizada completamente com 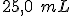 de uma solução
de uma solução 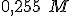 em
em ) . Qual é a concentração molar de
. Qual é a concentração molar de 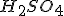 na água?
na água?