Química Geral ⇒ Fórmula Empírica
Moderador: [ Moderadores TTB ]
-
Cientista

- Mensagens: 1517
- Registrado em: Ter 19 Mar, 2013 16:23
- Última visita: 14-04-17
- Localização: Moçambique-Maputo
- Contato:
Abr 2016
13
01:00
Fórmula Empírica
Existem dois compostos binários de mercúrio com o oxigénio. O aquecimento de qualquer um deles resulta na decomposição dos mesmos, com a formação de mercúrio(puro) e oxigénio que se liberta. O aquecimento de 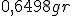 de um dos compostos deixa um resíduo de
de um dos compostos deixa um resíduo de 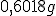 . Aquecendo
. Aquecendo 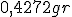 de outro composto resulta numa perda de massa de
de outro composto resulta numa perda de massa de 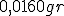 . Determine a fórmula empírica de cada composto.
. Determine a fórmula empírica de cada composto.
Última edição: Cientista (Qua 13 Abr, 2016 01:00). Total de 1 vez.
Força e bons estudos!
-
VALDECIRTOZZI

- Mensagens: 2569
- Registrado em: Seg 04 Ago, 2008 17:08
- Última visita: 13-10-20
Abr 2016
13
08:14
Re: Fórmula Empírica
Temos para o primeiro composto:
O seu aquecimento libera o oxigênio e o resíduo é mercúrio. então:
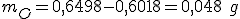
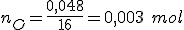
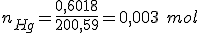
A fórmula fica: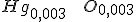 o que nos fornece:
o que nos fornece:  : óxido de mercúrio II (ou óxido mercúrico)
: óxido de mercúrio II (ou óxido mercúrico)
No segundo composto:
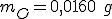
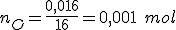
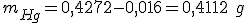
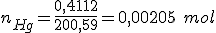
A fórmula fica: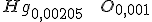 o que nos fornece:
o que nos fornece:  .
.
Isso me parece estranho, pois levá-nos a indicar que é o oxido de mercúrio I (òxido mercuroso), mas o cátion mercúrio I é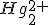 , o que nos leva à fórmula do óxido de mercúrio I sendo:
, o que nos leva à fórmula do óxido de mercúrio I sendo: 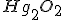 .
.
De qualquer modo...
Espero ter ajudado!
O seu aquecimento libera o oxigênio e o resíduo é mercúrio. então:
A fórmula fica:
No segundo composto:
A fórmula fica:
Isso me parece estranho, pois levá-nos a indicar que é o oxido de mercúrio I (òxido mercuroso), mas o cátion mercúrio I é
De qualquer modo...
Espero ter ajudado!
Última edição: VALDECIRTOZZI (Qua 13 Abr, 2016 08:14). Total de 1 vez.
So many problems, so little time!
-
Cientista

- Mensagens: 1517
- Registrado em: Ter 19 Mar, 2013 16:23
- Última visita: 14-04-17
- Localização: Moçambique-Maputo
- Contato:
Abr 2016
13
09:01
Re: Fórmula Empírica
Penso que, a ideia do exercício era determinar a fórmula empírica para a situação em I e em II, embora eu concorde com você, não tenha muito sentido, mas penso que o autor queria que se calculasse para cada caso.
Força e bons estudos!
-
- Tópicos Semelhantes
- Respostas
- Exibições
- Última msg
-
- 1 Respostas
- 812 Exibições
-
Última msg por Jigsaw
-
- 1 Respostas
- 614 Exibições
-
Última msg por Jigsaw
-
- 0 Respostas
- 717 Exibições
-
Última msg por FISMAQUIM
-
- 3 Respostas
- 1128 Exibições
-
Última msg por Jigsaw
-
- 2 Respostas
- 1524 Exibições
-
Última msg por JuliaHubble







