Resposta
Química Geral ⇒ Volume Parcial Molar Tópico resolvido
Moderador: [ Moderadores TTB ]
Jan 2014
12
18:53
Volume Parcial Molar
A 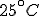 , a densidade de uma solução a
, a densidade de uma solução a 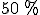 ponderais de etanol em água é de
ponderais de etanol em água é de 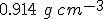 . Sabendo que o volume parcial molar da água neste solução é
. Sabendo que o volume parcial molar da água neste solução é 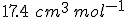 , determine o volume parcial molar do etanol?
, determine o volume parcial molar do etanol?
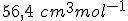 Como eu descubro o volume parcial molar do etanol?
Como eu descubro o volume parcial molar do etanol? 
Última edição: Kosoya (Dom 12 Jan, 2014 18:53). Total de 2 vezes.
Mar 2020
01
20:28
Re: Volume Parcial Molar
Bom, você já deve ter se formado mas antes tarde do que nunca.
Temos que 50% ponderais são de etanol, portanto são 50% de 1000g. (500g)
Chamaremos o Etanol de A e a Água de B.
Massa Molar etanol = 46g/mol → nA = m/MM :.
nA = 10,87 mol
Massa Molar água = 18g/mol → nB = m/MM :.
nB = 27,78 mol
(Esses dados de Massa Molar o problema não precisa fornecer pois são elementares).
d = m/v (densidade)
Vt = mt/d
Vt = 1000g / 0,914g/cm³
Vt = 1094,092cm³ (esse é o volume total da solução)
Vt = VpmA × nA + VpmB × nB (Equação de Gibbs)
1094,1cm³ = VpmA × 10,87mol + 17,4cm³/mol × 27,78mol
1094,1cm³ = 10,87mol × VpmA + 478,37cm³
Re-arranjando:
VpmA = (1094,1 - 478,37)cm³ / 10,87mol
:. VpmA ≈ 56,65 cm³/mol
Espero que a resposta seja satisfatória e desculpe a falta de organização estou fazendo pelo celular.
Temos que 50% ponderais são de etanol, portanto são 50% de 1000g. (500g)
Chamaremos o Etanol de A e a Água de B.
Massa Molar etanol = 46g/mol → nA = m/MM :.
nA = 10,87 mol
Massa Molar água = 18g/mol → nB = m/MM :.
nB = 27,78 mol
(Esses dados de Massa Molar o problema não precisa fornecer pois são elementares).
d = m/v (densidade)
Vt = mt/d
Vt = 1000g / 0,914g/cm³
Vt = 1094,092cm³ (esse é o volume total da solução)
Vt = VpmA × nA + VpmB × nB (Equação de Gibbs)
1094,1cm³ = VpmA × 10,87mol + 17,4cm³/mol × 27,78mol
1094,1cm³ = 10,87mol × VpmA + 478,37cm³
Re-arranjando:
VpmA = (1094,1 - 478,37)cm³ / 10,87mol
:. VpmA ≈ 56,65 cm³/mol
Espero que a resposta seja satisfatória e desculpe a falta de organização estou fazendo pelo celular.
A jornada agrega mais que o destino.
-
- Tópicos Semelhantes
- Respostas
- Exibições
- Última msg
-
- 0 Respostas
- 542 Exibições
-
Última msg por Uva1
-
- 1 Respostas
- 270 Exibições
-
Última msg por AlBrDe
-
- 5 Respostas
- 415 Exibições
-
Última msg por Argean
-
- 0 Respostas
- 260 Exibições
-
Última msg por fab12
-
- 1 Respostas
- 4985 Exibições
-
Última msg por Carlosft57








