(UFU-MG) Calcule a constante de equilíbrio [tex3]K_{p}[/tex3] da reação:
2[tex3]H_{2}[/tex3](g)+[tex3]S_{2}[/tex3][tex3](g)\rightarrow[/tex3] S[tex3]H_{2}[/tex3]S(g)
(obs: A seta indica equilíbrio)
a [tex3]750^{\circ}[/tex3]C, sabendo-se que o sistema em equilíbrio se encontra à pressão total de 15 atm e sendo as frações molares dos constituintes:
[tex3]H_{2}[/tex3]= 1/6
[tex3]S_{2}[/tex3]=1/3
[tex3]H_{2}[/tex3]S=1/2
Resp:. 1,8 [tex3]atm^{-1}[/tex3]
Química Geral ⇒ (UFU-MG) Equilíbrio químico Tópico resolvido
- pklaskoski

- Mensagens: 104
- Registrado em: 28 Jun 2014, 14:19
- Última visita: 24-07-17
- Agradeceu: 65 vezes
- Agradeceram: 5 vezes
Jul 2014
19
11:32
(UFU-MG) Equilíbrio químico
Editado pela última vez por pklaskoski em 19 Jul 2014, 11:32, em um total de 1 vez.
- VALDECIRTOZZI

- Mensagens: 2569
- Registrado em: 04 Ago 2008, 17:08
- Última visita: 13-10-20
- Agradeceu: 197 vezes
- Agradeceram: 1590 vezes
Jul 2014
21
09:33
Re: (UFU-MG) Equilíbrio químico
Temos o sistema em equilíbrio:
}+S_2_{(g)}\rightleftharpoons 2 H_2S_{(g)})
A expressão da constante de equilíbrio do sistema é dada por:
}}{p^2_{H_2}_{(g)}\cdot p_{S_2}_{(g)}}) , onde
, onde 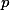 representa a pressão parcial de cada substância no equilíbrio.
representa a pressão parcial de cada substância no equilíbrio.
Sabemos também que: , ou seja, que a pressão parcial de uma substância genérica
, ou seja, que a pressão parcial de uma substância genérica 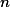 é o produto de sua fração molar
é o produto de sua fração molar ) pela pressão total
pela pressão total 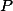 .
.
}=\frac{1}{2} \cdot P)
}=\frac{1}{6} \cdot P)
}=\frac{1}{3} \cdot P)
Substituindo esses resultados na expressão da constante de equilíbrio:
}}{p^2_{H_2}_{(g)}\cdot p_{S_2}_{(g)}})
^2}{\left(\frac{1}{6}\cdot P\right)^2 \cdot \left(\frac{1}{3}\cdot P\right)})


Espero ter ajudado!
A expressão da constante de equilíbrio do sistema é dada por:
Sabemos também que:
Substituindo esses resultados na expressão da constante de equilíbrio:
Espero ter ajudado!
Editado pela última vez por VALDECIRTOZZI em 21 Jul 2014, 09:33, em um total de 1 vez.
So many problems, so little time!
-
- Tópicos Semelhantes
- Resp.
- Exibições
- Últ. msg
-
- 1 Resp.
- 5036 Exibições
-
Últ. msg por MatheusBorges
-
- 2 Resp.
- 2436 Exibições
-
Últ. msg por AugustoITA
-
- 1 Resp.
- 1295 Exibições
-
Últ. msg por MicheleAlves
-
- 1 Resp.
- 1751 Exibições
-
Últ. msg por MicheleAlves
-
- 1 Resp.
- 2877 Exibições
-
Últ. msg por VALDECIRTOZZI
