book escreveu: ↑Qua 17 Nov, 2021 07:47
O ácido tartárico (HOOC-CH(OH)-CH(OH)-COOH, massa molar = 150 g/mol) é um sólido branco e o principal ácido presente em vinhos. Sua solubilidade em água é igual a 133 g/100 g H
2O a 20 ºC. Um dos derivados do ácido tartárico é o sal de Rochelle (tartarato de potássio e sódio). A equação que representa a ionização total do ácido tartárico está representada
a seguir.
(Imagem no Anexo)
Considere uma solução aquosa de ácido tartárico de concentração 0,1 mol/L e pH inicial igual a 2, à qual foi adicionado
sal de Rochelle.
a) Após essa adição, o que acontecerá com o grau de ionização do ácido tartárico e com o pH dessa solução?
b) Considere o sistema formado pela adição de 0,6 mol de ácido tartárico a 80 g de água a 20 ºC. Utilizando os cálculos
adequados, classifique o sistema resultante como solução insaturada, solução saturada sem corpo de fundo ou solução
saturada com corpo de fundo
book,
Considere uma solução aquosa de ácido tartárico de concentração 0,1 mol/L e pH inicial igual a 2, à qual foi adicionado
sal de Rochelle.
a) Após essa adição, o que acontecerá com o grau de ionização do ácido tartárico e com o pH dessa solução?
A adição do tartarato de potássio e sódio (imagem abaixo)
aumentará a presença do íon comum, deslocando o equilíbrio para a esquerda (diminuindo o grau de ionização e aumentando o pH)
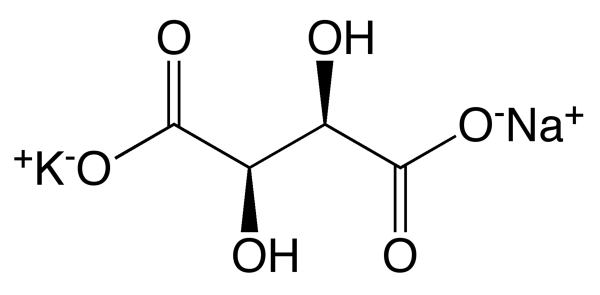
- 1200px-K-Na-L-(+)-tartrate.png (23.28 KiB) Exibido 851 vezes
b) Considere o sistema formado pela adição de 0,6 mol de ácido tartárico a 80 g de água a 20 ºC. Utilizando os cálculos adequados, classifique o sistema resultante como solução insaturada, solução saturada sem corpo de fundo ou solução saturada com corpo de fundo
Determinação da m de ácido tartárico em 100 g de H2O:
[tex3]\begin{cases}
0,60\ mol\times150\frac{g}{mol}\ (\text{ácido tartárico})=80\ g\ H_2O \\
x=100\ g
\end{cases}[/tex3]
[tex3]x=112,5g[/tex3]
Como a massa de ácido tartárico encontrada (112,5 g) é < 133 g para cada 100 g de H2O a solução é insaturada.









