Olá pessoal estou com muito dificuldade de fazer esse exercício....
(UFCE) A reação de fotossíntese é
}+6 \ H_2O_{(\ell)} \longrightarrow C_6H_{12}O_6{(s)} + 6 \ O_2{(g)})
. Estima-se que, em uma floresta tropical, cerca de
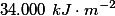
de energia solar são armazenados pelas plantas para realização da fotossíntese durante o período de um ano. A partir dos valores de entalpia-padrão de formação fornecidos a seguir, calcule:
Substância----------Entalpia-padrão de formação (
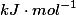
)
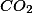
----------------- -394
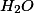
----------------- -286
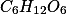
---------- -1275
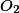
------------------- 0
A) A massa de
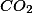
que será retirada da atmosfera por m² de floresta tropical durante o período de um ano?
B) A massa de
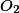
que será retirada da atmosfera por m² de floresta tropical durante o período de um ano?
OBS: Eu calculei a entalpia de formação e deu: -2805 e também calculei a massa de
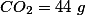
e também de
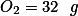
, Agora não sei como prosseguir.


