Veja, esta questão está um pouco confusa.
Inicialmente, se a massa molecular do hidrocarboneto é 58 g/mol , ele é o butano:

.
Por oxidação, é possível gerar o isobutanol
-CH_3)
e o n-butanol:

que são álcoois.
Também, por oxidação, pode gerar o ácido butanoico:
-OH)
Note que butano tem fórmula molecular
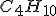
, que ambos os álcoois têm fórmula molecular
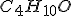
e que o ácido tem fórmula molecular
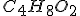
Em qualquer caso, ácido tem ponto de ebulição maior que os álcoois, pois forma pontes de hidrogênio mais fortes o que aumenta seu ponto de ebulição. Para ter certeza, verifiquei os valores de ponto de ebulição na literatura. Portanto a alternativa B está correta.
Na alternativa C, temos o problema:

Na combustão de 1 mol de
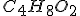
,
formam-se 4 mols de água que são 72 g. A alternativa está errada, pois diz que se
gastam 72 g de água. Na combustão o reagente, além do ácido, é o gás oxigênio, é ele que é gasto (consumido) durante a combustão.
Na alternativa D, além dos isômeros acima há o o álcool terc-butílico:
-OH)
A alternativa E está correta, pois se contarmos as ligações no ácido, veremos que há 13 ligações sigma e 1 pi.
Espero ter ajudado!









