Em um calorímetro adiabático, com capacidade térmica desprezível, são introduzidos, sob pressão constante de 1 atm, um volume V1 de solução aquosa 1,0 molar de ácido clorídrico e um volume V2 de solução aquosa 1,0 molar de hidróxido de sódio. A reação que ocorre é aquele representada pela equação química:
[tex3]H^{+}[/tex3]
(aq) + [tex3]OH^{-}[/tex3]
(aq) → [tex3]H_{2} O[/tex3]
(l)
As misturas efetuadas são as seguintes:
I- V1 = 100 ml e V2 = 100 ml e observa-se um aumento de temperatura ∆T1.
II- V1 = 50 ml e V2 = 150 ml e observa-se um aumento de temperatura ∆T2.
III- V1 = 50 ml e V2 = 50 ml e observa-se um aumento de temperatura ∆T3.
Com relação ao efeito térmico que se observa, é correto
prever que:
a) ∆T1 ≅ ∆T3 > ∆T2
b) ∆T1 > ∆T2 > ∆T3
c) ∆T1 > ∆T2 ≅ ∆T3
d) ∆T1 > ∆T3 > ∆T2
e) ∆T1 ≅ ∆T3 ≅ ∆T2
Olá, Comunidade!
Vocês devem ter notado que o site ficou um período fora do ar (do dia 26 até o dia 30 de maio de 2024).
Consegui recuperar tudo, e ainda fiz um UPGRADE no servidor! Agora estamos em um servidor dedicado no BRASIL!
Isso vai fazer com que o acesso fique mais rápido (espero )
)
Já arrumei os principais bugs que aparecem em uma atualização!
Mas, se você encontrar alguma coisa diferente, que não funciona direito, me envie uma MP avisando que eu arranjo um tempo pra arrumar!
Vamos crescer essa comunidade juntos
Grande abraço a todos,
Prof. Caju
Vocês devem ter notado que o site ficou um período fora do ar (do dia 26 até o dia 30 de maio de 2024).
Consegui recuperar tudo, e ainda fiz um UPGRADE no servidor! Agora estamos em um servidor dedicado no BRASIL!
Isso vai fazer com que o acesso fique mais rápido (espero
Já arrumei os principais bugs que aparecem em uma atualização!
Mas, se você encontrar alguma coisa diferente, que não funciona direito, me envie uma MP avisando que eu arranjo um tempo pra arrumar!
Vamos crescer essa comunidade juntos
Grande abraço a todos,
Prof. Caju
IME/ITA ⇒ (ITA 1995) Termoquimica
Moderador: [ Moderadores TTB ]
-
kevin22

- Mensagens: 63
- Registrado em: 04 Out 2013, 07:21
- Última visita: 16-02-17
- Agradeceram: 3 vezes
Ago 2014
23
18:21
(ITA 1995) Termoquimica
Editado pela última vez por kevin22 em 23 Ago 2014, 18:21, em um total de 1 vez.
-
VALDECIRTOZZI

- Mensagens: 2569
- Registrado em: 04 Ago 2008, 17:08
- Última visita: 13-10-20
- Agradeceu: 197 vezes
- Agradeceram: 1590 vezes
Ago 2014
25
10:35
Re: (ITA 1995) Termoquimica
Creio que a solução seja a seguinte:
A reação de neutralização entre um ácido e uma base forte exotérmica e assumamos a reação de neutralização entre 1 mol acido forte e 1 mol de base forte, formando água líquida tenha uma variação de entalpia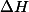 em kJ/mol de água
em kJ/mol de água
No caso I, houve a reação de de 0,1 mol de ácido com 0,1 mol de base, formando 0,1 mol de água. A energia liberada será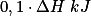 . Como o volume total da solução é
. Como o volume total da solução é 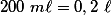 , temos que a quantidade de calor liberada por litro de solução será:
, temos que a quantidade de calor liberada por litro de solução será: 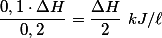 .
.
No caso II, houve a reação de de 0,05 mol de ácido com 0,15 mol de base, formando 0,05 mol de água. A energia liberada será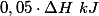 . Como o volume total da solução é
. Como o volume total da solução é 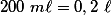 , temos que a quantidade de calor liberada por litro de solução será:
, temos que a quantidade de calor liberada por litro de solução será: 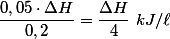 .
.
No caso III, houve a reação de de 0,05 mol de ácido com 0,05 mol de base, formando 0,05 mol de água. A energia liberada será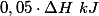 . Como o volume total da solução é
. Como o volume total da solução é 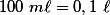 , temos que a quantidade de calor liberada por litro de solução será:
, temos que a quantidade de calor liberada por litro de solução será: 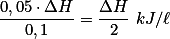 .
.
Dessa forma, é possível concluir que a alternativa A é a correta.
Espero ter ajudado!
A reação de neutralização entre um ácido e uma base forte exotérmica e assumamos a reação de neutralização entre 1 mol acido forte e 1 mol de base forte, formando água líquida tenha uma variação de entalpia
No caso I, houve a reação de de 0,1 mol de ácido com 0,1 mol de base, formando 0,1 mol de água. A energia liberada será
No caso II, houve a reação de de 0,05 mol de ácido com 0,15 mol de base, formando 0,05 mol de água. A energia liberada será
No caso III, houve a reação de de 0,05 mol de ácido com 0,05 mol de base, formando 0,05 mol de água. A energia liberada será
Dessa forma, é possível concluir que a alternativa A é a correta.
Espero ter ajudado!
Editado pela última vez por VALDECIRTOZZI em 25 Ago 2014, 10:35, em um total de 1 vez.
So many problems, so little time!
-
- Tópicos Semelhantes
- Respostas
- Exibições
- Última mensagem
-
- 2 Respostas
- 4618 Exibições
-
Última mensagem por gabrielifce
-
- 3 Respostas
- 3195 Exibições
-
Última mensagem por viniciusrts
-
- 1 Respostas
- 2267 Exibições
-
Última mensagem por VALDECIRTOZZI
-
- 1 Respostas
- 1830 Exibições
-
Última mensagem por Jigsaw
