Bom amigo, temos a seguinte reação ocorrendo:
%7D%20+I_%7B2(g)%7D%20%5Crightarrow%20%20ZnI_%7B2(s))
Note que a proporção estequiométrica é de 1:1:1.
É uma questão típica de reagente limitante ou excesso. Note que do enunciado já temos o limitante: iodo, e o em excesso foi o zinco(pois esse acaba sobrando).
Portanto, todas as 5g de iodo foi consumido, assim você tem:
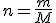
onde n é o número de mols, m é a massa utilizada e M a massa molecular do composto.
Para saber quantos mols de iodo(M = 126,9x2 = 253,8u) reagiram temos:
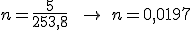
mols de iodo.
Como a proporção estequiométrica é de 1:1:1 podemos concluir que também reagiram 0,0197 mols de zinco( M = 65,4 u). Para achar a massa de zinco que reagiu fazemos:
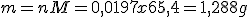
de zinco reagiu.
Como inicialmente tinhamos
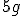
Sobrou
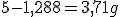
sobraram.
Então é isso amigo, falow!
"Ainda que eu falasse a língua dos homens e falasse a língua dos anjos, sem amor eu nada seria."