Na(s) questão(ões) a seguir escreva nos parênteses a letra (V) se a afirmativa for verdadeira ou (F) se a afirmativa for falsa;
Um determinado defensivo agrícola, quando exposto ao meio ambiente, decompõe-se através de uma reação química. Considerando que a velocidade de decomposição medida em laboratório apresentou os resultados a seguir:
Concentração Inicial (g/l) --------- Velocidade inicial de decomposição (g/l/mês)
0,1 ---------------------------------------- 0,002
0,2 ---------------------------------------- 0,004
0,6 ---------------------------------------- 0,012
Analise as afirmativas a seguir (verdadeira "V" ou falsa "F"):
( ) A decomposição deste defensivo segue uma cinética de segunda ordem.
( ) O Tempo para que a concentração do defensivo se reduza a valores despresíveis independe de sua concentração inicial.
( ) A constante de decomposição do defensivo é de 0,02 [tex3]mes^{-1}[/tex3]
.
( ) O tempo de meia vida do defensivo é de [0,02/ln(2)] mês.
( ) A velocidade inicial de decomposição do defensivo é de 0,006 g/L/mês para uma concentração inicial de 0,3 g/L.
Resposta: FVVFV
Se alguém puder responder, agradeço.
Físico-Química ⇒ (UFPE) Cinética Química Tópico resolvido
Moderador: [ Moderadores TTB ]
Dez 2013
23
20:50
(UFPE) Cinética Química
Última edição: lehhco (Seg 23 Dez, 2013 20:50). Total de 2 vezes.
-
VALDECIRTOZZI

- Mensagens: 2569
- Registrado em: Seg 04 Ago, 2008 17:08
- Última visita: 13-10-20
Dez 2013
24
10:07
Re: (UFPE) Cinética Química
Chamando de ![[A_o] [A_o]](https://www.tutorbrasil.com.br/latex/mimetex_.cgi?%5BA_o%5D) a concentração inicial do defensivo agrícola, podemos escrever para a reação dada:
a concentração inicial do defensivo agrícola, podemos escrever para a reação dada:
![v=k \cdot [A_o]^n v=k \cdot [A_o]^n](https://www.tutorbrasil.com.br/latex/mimetex_.cgi?v=k%20%5Ccdot%20%5BA_o%5D%5En) , onde
, onde 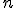 é a oredem da reação:
é a oredem da reação:
temos:
![0,002=k\cdot[0,1]^n \ (I) 0,002=k\cdot[0,1]^n \ (I)](https://www.tutorbrasil.com.br/latex/mimetex_.cgi?0,002=k%5Ccdot%5B0,1%5D%5En%20%5C%20(I))
![0,004=k \cdot [0,2]^n \ (II) 0,004=k \cdot [0,2]^n \ (II)](https://www.tutorbrasil.com.br/latex/mimetex_.cgi?0,004=k%20%5Ccdot%20%5B0,2%5D%5En%20%5C%20(II))
Dividindo as equações acima membro a membro temos:
![\frac{0,002}{0,004}=\frac{k \cdot[0,1]^n}{k \cdot[0,2]^n} \frac{0,002}{0,004}=\frac{k \cdot[0,1]^n}{k \cdot[0,2]^n}](https://www.tutorbrasil.com.br/latex/mimetex_.cgi?%5Cfrac%7B0,002%7D%7B0,004%7D=%5Cfrac%7Bk%20%5Ccdot%5B0,1%5D%5En%7D%7Bk%20%5Ccdot%5B0,2%5D%5En%7D)
%5En)
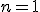
A reação é de primeira ordem.
Como a velocidade dobra ao dobrarmos a concentração incial, triplica se triplicarmos a concentração incial e assim por diante; o tempo para chegarmos a concentrações desprezíveis é independente da concentração inicial.
Como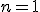 , podemos calcular
, podemos calcular  , usando, por exemplo, a primeira equação:
, usando, por exemplo, a primeira equação:
![0,002=k \cdot[0,1]^1 0,002=k \cdot[0,1]^1](https://www.tutorbrasil.com.br/latex/mimetex_.cgi?0,002=k%20%5Ccdot%5B0,1%5D%5E1)
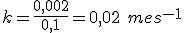
Uma equação de primeira ordem pode assumir a seguinte forma, quando se utiliza métodos de cálculo integral:
![\ln \frac{[R_t]}{[R_0]}=-kt \ln \frac{[R_t]}{[R_0]}=-kt](https://www.tutorbrasil.com.br/latex/mimetex_.cgi?%5Cln%20%5Cfrac%7B%5BR_t%5D%7D%7B%5BR_0%5D%7D=-kt) , onde
, onde ![[R_t] [R_t]](https://www.tutorbrasil.com.br/latex/mimetex_.cgi?%5BR_t%5D) é concentração da espécie num dado tempo
é concentração da espécie num dado tempo  . No nosso caso queremos que
. No nosso caso queremos que ![[A_t]=\frac{[A_o]}{2} [A_t]=\frac{[A_o]}{2}](https://www.tutorbrasil.com.br/latex/mimetex_.cgi?%5BA_t%5D=%5Cfrac%7B%5BA_o%5D%7D%7B2%7D) , porque o tempo de meia vida
, porque o tempo de meia vida  é o tempo necessário para que a concentração incial da espécie se reduza à metade.:
é o tempo necessário para que a concentração incial da espécie se reduza à metade.:
![\ln\frac{[A_t]}{[A_o]}=-k\cdot t_{\frac{1}{2}}} \ln\frac{[A_t]}{[A_o]}=-k\cdot t_{\frac{1}{2}}}](https://www.tutorbrasil.com.br/latex/mimetex_.cgi?%5Cln%5Cfrac%7B%5BA_t%5D%7D%7B%5BA_o%5D%7D=-k%5Ccdot%20t_%7B%5Cfrac%7B1%7D%7B2%7D%7D%7D)
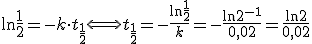
Se![[A_o]=0,3 \ g/\ell [A_o]=0,3 \ g/\ell](https://www.tutorbrasil.com.br/latex/mimetex_.cgi?%5BA_o%5D=0,3%20%5C%20g/%5Cell)
![v=0,02 \cdot[0,3]^1=0,006 \ g/\ell/mes v=0,02 \cdot[0,3]^1=0,006 \ g/\ell/mes](https://www.tutorbrasil.com.br/latex/mimetex_.cgi?v=0,02%20%5Ccdot%5B0,3%5D%5E1=0,006%20%5C%20g/%5Cell/mes)
Espero ter ajudado!
temos:
Dividindo as equações acima membro a membro temos:
A reação é de primeira ordem.
Como a velocidade dobra ao dobrarmos a concentração incial, triplica se triplicarmos a concentração incial e assim por diante; o tempo para chegarmos a concentrações desprezíveis é independente da concentração inicial.
Como
Uma equação de primeira ordem pode assumir a seguinte forma, quando se utiliza métodos de cálculo integral:
Se
Espero ter ajudado!
Última edição: VALDECIRTOZZI (Ter 24 Dez, 2013 10:07). Total de 2 vezes.
So many problems, so little time!
-
- Tópicos Semelhantes
- Respostas
- Exibições
- Última msg








