Pessoal, me desculpem se já houver um tópico sobre o assunto. Eu fiz uma busca e não encontrei.
A obtenção do alumínio a partir de seu minério é feita com o uso de energia elétrica, por meio de eletrólise, demandando uma grande quantidade de energia.
Já a extração do ferro, é feita pela reação entre o minério de ferro e carbono, a alta temperatura, com a liberação de monóxido de carbono, se não estou enganada.
Porque não é possível obter o alumínio metálico da mesma forma que se obtém o ferro?
Físico-Química ⇒ Produção de Alumínio Metálico Tópico resolvido
Moderador: [ Moderadores TTB ]
-
VALDECIRTOZZI

- Mensagens: 2569
- Registrado em: Seg 04 Ago, 2008 17:08
- Última visita: 13-10-20
Nov 2012
22
12:49
Re: Produção de Alumínio Metálico
Caroline, creio que a resposta passa por várias abordagens:
Primeiro, o alumínio ao ser aquecido, em condições de pouco controle, simplesmente queima, voltatiliza-se. As condições de um forno do tipo alto-forno (que é utilizado para se obter o fero gusa) não ajudam muito.
Segundo, a reação de obtenção do ferro metálico a partir do coque é uma reação de óxido-redução, da mesma forma que seria obter o alumínio da alumina (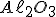 . Só que o potencial de redução do alumínio é um dos mais baixos entre os metais (apenas os metais alcalinos e alcalinos terrosos são mais baixos) o que dificulta muito a reação de redução dele por coque ou outro material.
. Só que o potencial de redução do alumínio é um dos mais baixos entre os metais (apenas os metais alcalinos e alcalinos terrosos são mais baixos) o que dificulta muito a reação de redução dele por coque ou outro material.
Por fim, a alumina é uma cerâmica que só se funde a mais de 2000°C, dá para imaginar a dificuldade de se conseguir essa temperatura e o gasto de energia para a produção de toneladas de alumínio que são necessárias?
Por isso, utiliza-se o processo Hall que mistura à bauxita a criolita (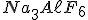 ) que abaixa o ponto de fusão da alumina para 950°C e é então eletrolisada.
) que abaixa o ponto de fusão da alumina para 950°C e é então eletrolisada.
Espero ter ajudado.
Primeiro, o alumínio ao ser aquecido, em condições de pouco controle, simplesmente queima, voltatiliza-se. As condições de um forno do tipo alto-forno (que é utilizado para se obter o fero gusa) não ajudam muito.
Segundo, a reação de obtenção do ferro metálico a partir do coque é uma reação de óxido-redução, da mesma forma que seria obter o alumínio da alumina (
Por fim, a alumina é uma cerâmica que só se funde a mais de 2000°C, dá para imaginar a dificuldade de se conseguir essa temperatura e o gasto de energia para a produção de toneladas de alumínio que são necessárias?
Por isso, utiliza-se o processo Hall que mistura à bauxita a criolita (
Espero ter ajudado.
Última edição: VALDECIRTOZZI (Qui 22 Nov, 2012 12:49). Total de 1 vez.
So many problems, so little time!
-
- Tópicos Semelhantes
- Respostas
- Exibições
- Última msg
-
- 1 Respostas
- 2866 Exibições
-
Última msg por joaopcarv
-
- 0 Respostas
- 969 Exibições
-
Última msg por goncalves3718
-
- 0 Respostas
- 1112 Exibições
-
Última msg por mah123
-
- 5 Respostas
- 664 Exibições
-
Última msg por questions
-
- 0 Respostas
- 388 Exibições
-
Última msg por carlosalves10








