O vinagre é uma solução aquosa que contém ácido acético. O equilíbrio químico envolvido nessa solução é apresentado na equação:
CH3COOH (aq) + H2O (ℓ) [tex3]\rightarrow[/tex3]
H3O+ (aq) + CH3COO– (aq) Ka = 2 ×10–5
Calcule o pH da solução de vinagre com concentração de ácido acético 0,05 mol/L.
Físico-Química ⇒ (FAMECA-2013) pH Tópico resolvido
Moderador: [ Moderadores TTB ]
Out 2014
27
18:25
(FAMECA-2013) pH
Última edição: natalia19 (Seg 27 Out, 2014 18:25). Total de 1 vez.
-
VALDECIRTOZZI

- Mensagens: 2569
- Registrado em: Seg 04 Ago, 2008 17:08
- Última visita: 13-10-20
Nov 2014
18
13:59
Re: (FAMECA-2013) pH
Temos que:
![k_a=\frac{[H_3O^+] \cdot [CH_3COO^-]}{[CH_3COOH]} k_a=\frac{[H_3O^+] \cdot [CH_3COO^-]}{[CH_3COOH]}](https://www.tutorbrasil.com.br/latex/mimetex_.cgi?k_a=%5Cfrac%7B%5BH_3O%5E+%5D%20%5Ccdot%20%5BCH_3COO%5E-%5D%7D%7B%5BCH_3COOH%5D%7D)
No equilíbrio:![[H_3O^+]=[CH_3COOH]=x [H_3O^+]=[CH_3COOH]=x](https://www.tutorbrasil.com.br/latex/mimetex_.cgi?%5BH_3O%5E+%5D=%5BCH_3COOH%5D=x) e que
e que ![[CH_3COOH]=0,05-x \approx 0,05 \ mol/\ell [CH_3COOH]=0,05-x \approx 0,05 \ mol/\ell](https://www.tutorbrasil.com.br/latex/mimetex_.cgi?%5BCH_3COOH%5D=0,05-x%20%5Capprox%200,05%20%5C%20mol/%5Cell) .
.
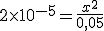
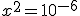

![pH=-\log [H_3O^+] pH=-\log [H_3O^+]](https://www.tutorbrasil.com.br/latex/mimetex_.cgi?pH=-%5Clog%20%5BH_3O%5E+%5D)

Espero ter ajudado!
No equilíbrio:
Espero ter ajudado!
Última edição: VALDECIRTOZZI (Ter 18 Nov, 2014 13:59). Total de 1 vez.
So many problems, so little time!
-
- Tópicos Semelhantes
- Respostas
- Exibições
- Última msg
-
- 2 Respostas
- 2468 Exibições
-
Última msg por BrunoAlves
-
- 1 Respostas
- 796 Exibições
-
Última msg por petras
-
- 1 Respostas
- 758 Exibições
-
Última msg por petras
-
- 1 Respostas
- 771 Exibições
-
Última msg por Jigsaw
-
- 1 Respostas
- 1270 Exibições
-
Última msg por jedibli








