Quando a sacarose é dissolvida em água, na
presença de um catalisador ácido, reage de acordo
com a equação representada abaixo, com uma lei de
velocidade V = k.[C12H22O11]. Se uma massa inicial
de 50 g de sacarose reduz-se para 45 g em 1,50
horas, na presença de uma determinada concentração de ácido clorídrico, qual é a meia-vida
para esta reação nas condições indicadas?
Dado: log2=0,3; log3=0,48;
----------------------H+
C12H22O11 + H2O [tex3]\rightarrow[/tex3]
C6H12O6 + C6H12O6
Sacarose------Agua-----Glicose-----Frutose
A) 11,25 horas
B) 16,44 horas
C) 28,72 horas
D) 37,91 horas
E) 54,28 horas
gab: A
Físico-Química ⇒ (FACID 2013) cinetica quimica
Moderador: [ Moderadores TTB ]
-
xtremer4ce

- Mensagens: 3
- Registrado em: Dom 17 Mai, 2015 10:31
- Última visita: 18-05-15
Mai 2015
17
16:02
(FACID 2013) cinetica quimica
Última edição: xtremer4ce (Dom 17 Mai, 2015 16:02). Total de 1 vez.
-
VALDECIRTOZZI

- Mensagens: 2569
- Registrado em: Seg 04 Ago, 2008 17:08
- Última visita: 13-10-20
Mai 2015
20
09:55
Re: (FACID 2013) cinetica quimica
Como a reação é de primeira ordem, a constante de reação é dada por:
![k=-\frac{\ln\frac{\left[C_{12}H_{22}O_{11}\right]_{final}}{\left[C_{12}H_{22}O_{11}\right]_{inicial}}}{\Delta T} k=-\frac{\ln\frac{\left[C_{12}H_{22}O_{11}\right]_{final}}{\left[C_{12}H_{22}O_{11}\right]_{inicial}}}{\Delta T}](https://www.tutorbrasil.com.br/latex/mimetex_.cgi?k=-%5Cfrac%7B%5Cln%5Cfrac%7B%5Cleft%5BC_%7B12%7DH_%7B22%7DO_%7B11%7D%5Cright%5D_%7Bfinal%7D%7D%7B%5Cleft%5BC_%7B12%7DH_%7B22%7DO_%7B11%7D%5Cright%5D_%7Binicial%7D%7D%7D%7B%5CDelta%20T%7D)
![k=-\frac{2,303 \cdot\log\frac{\left[C_{12}H_{22}O_{11}\right]_{final}}{\left[C_{12}H_{22}O_{11}\right]_{inicial}}}{\Delta T} k=-\frac{2,303 \cdot\log\frac{\left[C_{12}H_{22}O_{11}\right]_{final}}{\left[C_{12}H_{22}O_{11}\right]_{inicial}}}{\Delta T}](https://www.tutorbrasil.com.br/latex/mimetex_.cgi?k=-%5Cfrac%7B2,303%20%5Ccdot%5Clog%5Cfrac%7B%5Cleft%5BC_%7B12%7DH_%7B22%7DO_%7B11%7D%5Cright%5D_%7Bfinal%7D%7D%7B%5Cleft%5BC_%7B12%7DH_%7B22%7DO_%7B11%7D%5Cright%5D_%7Binicial%7D%7D%7D%7B%5CDelta%20T%7D)
Como o logaritmo é um quociente, podemos usar apenas as massas de sacarose para o cálculo.
)
=0,06141%20%5C%20h%5E%7B-1%7D)
A meia vida de uma reação de primeira ordem é dada por:
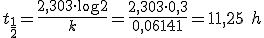
Espero ter ajudado!
Como o logaritmo é um quociente, podemos usar apenas as massas de sacarose para o cálculo.
A meia vida de uma reação de primeira ordem é dada por:
Espero ter ajudado!
Última edição: VALDECIRTOZZI (Qua 20 Mai, 2015 09:55). Total de 1 vez.
So many problems, so little time!
-
- Tópicos Semelhantes
- Respostas
- Exibições
- Última msg







